Относительная концентрация - молекула
Cтраница 1
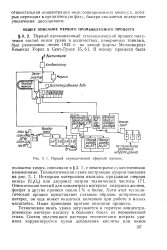 |
Первый периодический эфирный процесс. [1] |
Относительная концентрация недиссоцйированных молекул, к отб-рые переходят в органическую фазу, быстро снижается вследствие увеличения диссоциации. [2]
Таким образом, в верхней части сосуда относительная концентрация молекул тяжелой компоненты уменьшается, а легкой - увеличивается. [3]
В результате количество свободных молекул воды становится меньше, а относительная концентрация молекул сахара по отношению к оставшимся свободным молекулам воды возрастает. [4]
В результате этого количество свободных молекул воды становится меньше, а относительная концентрация молекул сахара по отношению к оставшимся свободным молекулам воды возрастает. [5]
 |
Качественная зависимость функции распределения. [6] |
Неравновесный режим распада реализуется в некоторой области значений температуры газа Т, давления р и относительной концентрации распадающихся молекул р; существуют верхние и нижние значения этих параметров, ограничивающие зону неравновесности. [7]
Неравновесный режим распада реализуется в некоторой области значений температуры газа Т, давления р и относительной концентрации распадающихся молекул г г, существуют верхние и нижние значения этих параметров, ограничивающие зону неравновесности. [8]
Ьсли в газовой смеси молекл-осцилляторов с атомами инертного газа можно пренебречь столкновениями молекул между собой ( малая относительная концентрация молекул), то кинетические уравнения для заселенностей х осцилляторов на уровне п выводятся из уравнений баланса процессов возбуждения и тушения под влиянием столкновений молекулы с частицами резервуара. [9]
Рассмотрим более подробно два предельных случая, представляющих практический интерес: однокомпонентную систему А и двукомпонентную систему А В с малой относительной концентрацией молекул А. [10]
Для сил притяжения р0; из приведенного уравнения мы видим, что когда абсолютная величина потенциальной энергии возрастает в арифметической прогрессии, то относительная концентрация молекул - возрастает в геометрической прогрессии. [11]
Практически в условиях механизма Sjvl может иметь место любой результат, начиная от полной рацемизации и кончая почти полным обращением конфигурации, в зависимости от того, насколько быстро после ионизации наступает нуклеофиль-ная атака. Наиболее часто рацемизация сопровождается некоторым обращением конфигурации, причем соотношение между ними для данного субстрата очень сильно зависит от условий проведения реакции. В тех случаях, когда растворитель может играть роль нуклеофила ( например, при использовании водных растворов), из-за очень высокой относительной концентрации молекул растворителя быстрая атака более вероятна, чем тогда, когда нуклеофильный реагент приходится специально до-б. В результате обращение конфигурации в первом случае проявляется в более сильной степени. Особенно эффективным в этом смысле является растворитель, обладающий высокой сольватирующей способностью, такой как, например, вода, поскольку такой растворитель значительно быстрее создает вокруг карбониевого иона сольватное окружение. [12]
Практически, в условиях механизма Sjvl может иметь место любой результат, начиная от полной рацемизации и кончая почти полным обращением конфигурации, в зависимости от того, насколько быстро после ионизации наступает нуклеофиль-ная атака. Наиболее часто рацемизация сопровождается некоторым обращением конфигурации, причем соотношение между ними для данного субстрата очень сильно зависит от условий проведения реакции. В тех случаях, когда растворитель может играть роль нуклеофила ( например, при использовании водных растворов), из-за очень высокой относительной концентрации молекул растворителя быстрая атака более вероятна, чем тогда, когда нуклеофильный реагент приходится специально до-б. В результате обращение конфигурации в первом случае проявляется в более сильной степени. Особенно эффективным в этом смысле является растворитель, обладающий высокой сольватирующей способностью, такой как, например, вода, поскольку такой растворитель значительно быстрее создает вокруг карбониевого иона сольватное окружение. [13]
Рассмотрим, как влияет гидратация на свойства растворов неэлектролитов, например сахара, в воде. Осмотическое давление возрастает у раствора сахара быстрее, чем это следует из роста концентрации. Для объяснения этого представим, что некоторая часть молекул воды соединяется с молекулами сахара. В результате количество свободных молекул воды становится меньше, а относительная концентрация молекул сахара по отношению к оставшимся свободным молекулам воды возрастает. [14]
 |
Зависимость логарифма обратной растворимости хлоридов щелочных металлов в воде, спиртах и ацетоне от природы катиона. Показано сильное влияние структуры воды на растворимость ионов. [15] |
Страницы: 1 2