Диаграмма - состояние - двухкомпонентная система
Cтраница 2
Диаграммы состояния двухкомпонентных систем InCls - МС1 и NaCl - МС1 ( где М - Ag, Co или №) в большинстве случаев характеризуются широкой областью растворимости компонентов в твердом состоянии. При зонной перекристаллизации указанной эвтектической смеси перечисленные хлориды обладают невысокими коэффициентами распределения; по-видимому, в тройных системах InCls - NaCl - МС1 области устойчивости твердых растворов уменьшаются. [16]
Плоскость диаграммы состояния двухкомпонентной системы делится на фазовые области, границами которых служат линии, пересекающиеся в точках. Число фаз в равновесной конденсированной изобарической системе, состоящей из двух компонентов, не может быть больше трех. Отсюда следует также, что в фазовых областях диаграмм состояния двухкомпо-нентных систем могут находиться либо одна, либо две фазы. Границы фазовых областей находят, определяя экспериментально положение разделяющих их линий моновариантных равновесий; эти линии пересекаются в точках инвариантных равновесий. [17]
На диаграмме состояния двухкомпонентных систем на оси абсцисс точками указываются составы сплавов, а на двух осях ординат ( каждая соответствует 100 % - ному содержанию одного из компонентов) - их температура. Любая точка на диаграмме определяет фазовый и химический составы сплава, а также его структуру при данной температуре. Вертикальная линия соответствует определенному химическому составу. [18]
Рассмотрим основные типы диаграмм состояния двухкомпонентных систем в координатах: температура начала кристаллизации - процентный состав. [19]
Рассмотрим основные типы диаграмм состояния двухкомпонентных систем в координатах: температура - процентный состав. [20]
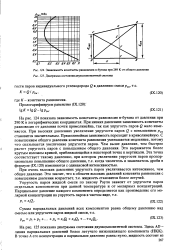 |
Зависимость константы равновесия н-бутана при 289 К от общего давления.| Диаграмма состояния двухкомпонентной системы. [21] |
На рис. 125 показана диаграмма состояния двухкомпонентной системы. [22]
 |
Диаграмма со - записать в виде. стояния двухкомпонентной системы с полиморф - расплав - аВ - - расплав - рВ ными превращениями л, on л. о компонентов. расплав - А р. - А уВ. [23] |
На рис. 23 показана диаграмма состояния двухкомпонентной системы, у которой один из компонентов - компонент В - имеет несколько полиморфных форм: а, р и у. Энантиотропные полиморфные превращения могут осуществляться как в твердом состоянии, так и в присутствии жидкой фазы. Если температура полного плавления смесей значительно изменяется в зависимости от количества добавляемого вещества, то на температуру полиморфного превращения одного из компонентов состав смеси не влияет. Поэтому переход между модификациями изображается изотермой, отвечающей температуре полиморфного превращения. [24]
 |
Диаграмма состояния двухкомпонентной системы с химическим соединением, плавящимся без разложения ( конгруэнтно. [25] |
На рис. 45 приведена диаграмма состояния двухкомпонентной системы с индивидуальным химическим соединением АВ, плавящимся без разложения. Эту диаграмму можно рассматривать как совокупность двух простейших двухкомпонентных диаграмм состояния с эвтектиками: одну - диаграмму системы А-АВ, в которой компонентами являются соединения А и АВ, и вторую - систему АВ-В с компонентами АВ и В. В соответствии с правилом определения конечных фаз кристаллизации все составы, лежащие влево от вертикали состава дв - АВ, заканчивают кристаллизоваться в эвтектике Е, а лежащие вправо - в эвтектике Е % Пути кристаллизации при этом аналогичны разобранным для двухкомпонентной диаграммы состояния с эвтектикой. [26]
На рис. 46 приведена диаграмма состояния двухкомпонентной системы с химическим соединением АВ, плавящимся с разложением. Характерной точкой этой диаграммы является инвариантная точка п перитектики. [27]
Наиболее типичными для таких диаграмм состояний двухкомпонентных систем являются температурные точки Т кр и Т р, называемые верхней и нижней критическими температурами взаимного неограниченного смешения ( растворения) двух жидкостей. [28]
В общем случае для построения диаграмм состояния двухкомпонентных систем пользуются тремя осями координат: t, р и с. При этом получаются пространственные модели. [29]
Страницы: 1 2 3 4 5