Коррозия - нержавеющая сталь
Cтраница 2
Скорость коррозии нержавеющей стали, рассчитанная на всю поверхность образца, была меньше примерно в четыре раза, чем скорость коррозии углеродистой стали. [16]
Процесс коррозии нержавеющих сталей в концентрированных О30 %) растворах HN03 с ванадатом идет при высоких положительных потенциалах по механизму перепассивации с преимущественным облегчением катодного процесса. [17]
 |
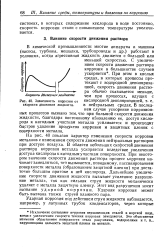
Коррозия металлов в контакте с титаном в морской воде при различном соотношении поверхностей металл SMe. титан STI. продолжительность испытаний 2500 ч. [18] |
Скорость коррозии нержавеющих сталей в контакте с катализаторами резко возросла. Высокая коррозионная стойкость титана подтверждена также испытаниями в промышленных условиях производства азотной кислоты. [19]
Сопротивление коррозии нержавеющих сталей обусловлено главным образом присутствием хрома. Влияние хрома ( не ниже 12 - 13 %) на повышение коррозионной стойкости связано с его способностью образовывать в окислительных средах на поверхности металла тонкий слой окиси. Никель ( второй основной легирующий компонент нержавеющих сталей) не только повышает коррозионную стойкость, но и позволяет получить высокие характеристики пластичности, вязкости и прочности при высоких температурах. [20]
Скорость коррозии нержавеющих сталей в контакте с катализаторами резко возросла. Высокая коррозионная стойкость титана была подтверждена также испытаниями в промышленных условиях производства азотной кислоты. [21]
Механизм коррозии нержавеющей стали в этом отношении пока остается недостаточно определенным, не имеется также работ по высоконикелевым сплавам инконель-600 и инколой-800. Мур и Джонс [56] нашли, что на углеродистой стали при рН 11 ( LiOH) основная пленка достигает определенной толщины и ее наружная поверхность имеет галькообразную структуру. Они интерпретировали этот результат как указание на то, что основная пленка одновременно генерируется на поверхности раздела металл - окись и растворяется на поверхности окись - раствор. Вначале контролирующей скорость стадией является реакция на поверхности раздела металл - окись, но окончательно контролирующей стадией становится процесс на поверхности окись - раствор. [22]
 |
Благородный металл.| Пассивный металл. [23] |
Скорость коррозии нержавеющей стали достигает максимума в 2 и. Катоды из нержавеющей стали не корродируют в серной кислоте небольших концентраций. Эти результаты отвечают механизму, предложенному выше. [24]
Процесс коррозии нержавеющих сталей еще более сложен. Скорость общей коррозии стали типа 18 - 8 в азотной кислоте весьма мала и не ею определяется срок службы, скажем, химического аппарата. Для этих сталей наиболее существенным является электрохимическое поведение таких структурных составляющих, как карбиды хрома, по отношению к твердому раствору железо - хром, которое приводит к так называемой межкристаллитной коррозии. [25]
Скорость коррозии нержавеющих сталей в окислителе указанного состава уже при содержании HF 0 5 % практически равна нулю. Однако если нержавеющая сталь предварительно подвергается нагреву, способствующему межкристаллитной коррозии ( 450 - Г-900 С), добавка HF к дымящей азотной кислоте усиливает коррозию. Алюминиевые сплавы в этих условиях абсолютно устойчивы. Стали, содержащие менее 15 % Сг ( без никеля), не защищаются HF в дымящей азотной кислоте. [26]
При этом коррозия нержавеющей стали имеет точечный характер. Она может быть использована в качестве конструкционного материала для реактора, подогревателя, холодильника, сборника для реакционной смеси и колонн отгонки аммиака и разложения хлоргидратов. [27]
Исключение составляет коррозия нержавеющих сталей в морской воде, когда с увеличением скорости течения коррозия замедляется. [29]
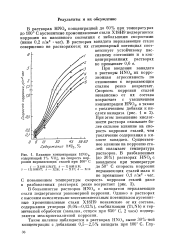 |
Влияние концентрации HN03, содержащей 1 % VOg, на скорость коррозии нержавеющих сталей при 100 С. [30] |
Страницы: 1 2 3 4 5