Коррозия - низколегированная сталь
Cтраница 2
 |
Скорость коррозии малолегированных н углеродистых сталей. [16] |
Ш-6) Особенно резко возрастает она при увеличении температуры свыше 400 С. Как указывалось выше ( см. табл. 1 - 5 и 1 - 6), при постоянной температуре давление воды и пара на скорость коррозии низколегированных сталей не влияет. Снижается она более чем в два раза за первые 250 - 500 час испытаний у сталей, легированных 5t % хрома. [17]
При относительно м-алой аэрации ( например, в спокойной воде) нержавеющая сталь находится в малоустойчивом пассивном состоянии, поэтому она является малоэффективным катодом, способным лишь немного ускорить коррозию железных сплавов: и более заметно - сплавов с более отрицательным потенциалом, подобных алюминию. Так, например, допустимо применение заклепок или сварных швов из нержавеющей стали, имеющих относительно небольшую площадь, на листах обшивки из низколегированной стали. В этом случае нержавеющая сталь остается вполне устойчивой благодаря электрохимическому защитному эффекту катодной поляризации и лишь IB очень небольшой степени увеличивает общую скорость коррозии низколегированной стали. [18]
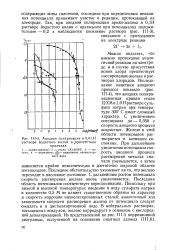 |
Анодная поляризация в 0 01 Н. [19] |
Последнее обстоятельство указывает на то, что железо переходит в пассивное состояние. С дальнейшим ростом потенциала скорость растворения железа вновь увеличивается. Последняя область потенциалов соответствует перепассивации. Поскольку при низкой и высокой температурах введение в воду сульфата натрия в количестве 0 5 М не влияет существенным образом на характер и скорость коррозии низколегированных сталей; аналогичный ход зависимости скорости растворения железа от потенциала следует ожидать и в дистиллированной воде. В нейтральных растворах, насыщенных воздухом, железо корродирует в основном с кислородной деполяризацией. [20]
Сталь в этом случае находится в пассивном состоянии, что и обусловливает в ней снижение скорости коррозии. Однако вследствие значительного содержания кислорода в воде скорость катодного процесса велика и стационарный потенциал стали-уже близок к потенциалу пробоя. Из-за флуктуации потенциала отдельные участки поверхности стали попадают в область перепассивации, что связано с возрастанием скорости растворения металла на этих участках и появлением язв. Очевидно, это обстоятельство связано с уменьшением рН среды. В потоке воды со скоростью 0 4 м / сек при температуре 310 С скорость коррозии низколегированных сталей, измеренная по количеству выделившегося водорода, равна скорости их в стати - ческих условиях. [21]
Страницы: 1 2