Коррозия - перлитная сталь
Cтраница 1
Коррозия перлитных сталей в водных средах имеет электрохимическую природу. Одним из основных факторов, определяющих характер и интенсивность коррозии перлитных сталей, является содержание растворенного кислорода в воде. При этом кислород выполняет двойственную роль. С одной стороны, он служит мощным деполяризатором катодных участков коррозионных пар и тем самым ускоряет протекание коррозии при условии, если катодный процесс является контролирующим фактором. С другой стороны, кислород, окисляя металл, повышает стабильность защитных пленок и, следовательно, может даже снижать скорость коррозии. Чем выше концентрация кислорода в растворе, тем больше возможность образования прочных защитных пленок на поверхности стали и более благородным становится электродный потенциал. Участки металла, получающие больше кислорода, выполняют роль катода по отношению к участкам поверхности металла, которые омываются водой с малой концентрацией кислорода, и вследствие этого возникает так называемая макрогальванопара неравномерной аэрации. [1]
Скорость коррозии перлитной стали резко снижается. Нейтральный водный режим требует очень чистой, не содержащей СО2 питательной воды; отсутствия в питательном тракте элементов, выполненных из меди и медесодержа-щих сплавов. [2]
Глубина коррозии перлитных сталей 12Х1МФ и 12Х2МФСР в поташе при 540 С примерно на уровне коррозии в продуктах сгорания природного газа, в то время как в интервале температур 570 - 590 С происходит резкое увеличение интенсивности коррозии. [3]
Общий характер коррозии перлитных сталей 12Х1МФ и 12Х2МФСР почти одинаков. [4]
Другим способом снижения коррозии перлитных сталей является дозированный ввод в движущуюся химически обессоленную воду кислорода. Скорость доставки кислорода к поверхности металла через диффузионный слой пропорциональна коэффициенту его диффузии. Коэффициент турбулентной диффузии кислорода превосходит коэффициент его молекулярной диффузии, благодаря чему движение воды облегчает доставку кислорода к поверхности раздела фаз и увеличивает его концентрацию у поверхности металла. Последнее обстоятельство облегчает адсорбцию кислорода и приводит к увеличению стационарного потенциала железа. [5]
Начиная с температуры 600 С процесс коррозии перлитных сталей под влиянием золы березовского угля существенным образом ускоряется. [6]
В блоках сверхкритических давлений из вредно воздействующих на коррозию перлитных сталей газов в питательную воду поступает только кислород - за счет присоса воздуха в вакуумных системах и контакта с воздухом в системе подготовки добавочной воды. Содержание кислорода в питательной воде в связи с этим нормируется довольно жестко ( табл. 1 - 3) и должно обеспечиваться главным образом за счет термической деаэрации. [7]
Таким образом, температура наиболее сильно влияет на ускорение процесса коррозии перлитных сталей в воздухе в области образования на их поверхности трехслойной оксидной пленки. [8]
 |
Коррозионная стойкость. [9] |
Для расчетов содержания продуктов коррозии в водном теплоносителе существенную роль играют закономерности, определяющие вынос продуктов коррозии перлитных сталей с поверхности корродирующего металла в смывающую его среду. [10]
 |
Коррозия аустенитных сталей в химически обессоленой воде.| Скорость перехода продуктов коррозии в воду. [11] |
Для расчетов содержания продуктов коррозии в водном теплоносителе существенную роль играют закономерности, определяющие вынос ( переход) продуктов коррозии перлитных сталей с поверхности корродирующего металла в смывающую их среду. [12]
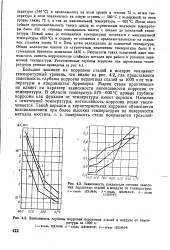 |
Зависимость показателя степени окисления перлитных сталей в воздухе от температуры.| Зависимость глубины коррозии перлитных сталей в воздухе от температуры за 1000 ч. [13] |
Большое влияние на коррозию сталей в воздухе оказывает температурный уровень, что видно из рис. 4.2, где представлена зависимость глубины коррозии перлитных сталей за 1000 ч от температуры в координатах Аррениуса. Марка стали практически не влияет на характер зависимости интенсивности коррозии от температуры. В области температур 570 - 600 С кривые глубины коррозии как функции от температуры имеют перелом. Начиная с отмеченной температуры, интенсивность коррозии резко увеличивается. [14]
В потоке химически обессоленной воды при концентрации кислорода, близкой к 0 3 мг / кг, перлитная сталь при температуре 80 С находится в пассивном состоянии. Обычно для снижения скорости коррозии перлитных сталей в химически обессоленную воду вводят кислород в количестве 0 2 мг / кг. В реальных контурах всегда могут быть застойные зоны, где при концентрации кислорода свыше 0 2 мг / кг коррозия интенсифицируется. [15]
Страницы: 1 2