Анодная коррозия
Cтраница 3
Бели благородные примеси залегают в основном металле или снова осаждаются на нем в процессе коррозии, то выделение водорода происходит у этих примесей, как катодов, а основной металл подвергается анодной коррозии в точках, непосредственно их окружающих. [31]
Если для катодной защиты от коррозии требуется лишь небольшой защитный ток порядка 10 мА, то плюсовую клемму преобразователя защитной установки можно подключить к заземлению станции Е, при условии, что нет оснований опасаться существенной анодной коррозии за-землителя и подключенного к нему оборудования. При большем требуемом защитном токе на станциях ( подстанциях) могут быть предусмотрены дополнительные защитные установки с анодными заземлителями А, которые устраняют анодную нагрузку на заземлители станции. КЕ или заземлитель станции Е на станции нужно иметь преобразователи защитных установок с низким напряжением на выходе и большим защитным током. При разъединительных устройствах типов в-д станции катодной защиты от коррозии могут быть размещены по трассе независимо от требуемой величины тока для защиты стальных труб. [32]
На другие подземные трубопроводы, пересекающиеся в области воронки напряжений с трубопроводами, имеющими катодную защиту, за пределами воронки напряжений натекает защитный ток, стекающий с них в области катодной воронки напряжений, вызывая там анодную коррозию. Потенциал незащищенного трубопровода ( испытывающего влияние), измеренный при помощи электрода сравнения над местом пересечения, представляет собой в основном омическое падение напряжения, вызванное защитным током, текущим в грунте к дефекту изоляции трубопровода с катодной защитой. На рис. 10.16 схематически показано распределение потенциалов в грунте, характер воронки напряжений и распределение потенциалов на другом трубопроводе, испытывающем влияние системы катодной защиты. [33]
Если например, погрузить в раствор хлористого калия свинцовую пластину с помещенной на ней линзой или часовым стеклом, то кольцеобразная поверхность щели вокруг контактной точки начинает травиться или же на ней появляется питтинг, типичный для анодной коррозии; в то же время на поверхности за этой щелью появляются слабые цвета интерференции, характерные для катодных участков ( фиг. Если опыт продолжается долгое время, то, как показал Фелпс4, щелочь, образовавшаяся во внешней зоне, начинает действовать на свинец, давая кольцо красной свинцовой окиси, вероятно, образующейся в результате гидролиза плумбита. [34]
Растворы гидроокисей щелочных металлов также вызывают оррозию олова, причем обыч-но образуются станнаты. При анодной коррозии могут также образовываться, ленки, приводящие к пассивированию. [35]
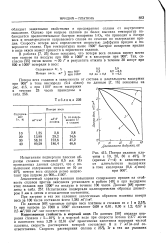 |
Потери сплавов платины с 10, 20, 30 и 40 % 1г ( кривые 1 - 4 в зависимости от длительности выдержки в токе кислорода ( 0 4 л / мин при 900. [36] |
По данным [50] анодная коррозия сплавов с 5 - 10 % т в морской воде при скорости потока 2 377 м / сек и плотности тока 3 28 и 32 81 а / ж2 практически идентична коррозии чистой платины, скорость растворения которой составляет 8 и 7 мГ / а-год соответственно. [37]
В растворах, содержащих ионы хлора или фтора, окисная пленка разрыхляется и возможна коррозия анода. В присутствии ионов NOg анодная коррозия циркония уменьшается. [38]
В работе Ландера отмечается возможность непосредственного окисления анодно поляризуемого свинца молекулами воды. Отмечается также влияние структуры пленки двуокиси свинца на скорость анодной коррозии. Рост коррозии при повышении температуры объясняется автором не только влиянием температуры на скорость процесса окисления металла, но и увеличением пористости анодной пленки. [39]
Наибольшее влияние на потенциал других трубопроводов и кабелей обычно оказывают воронки напряжения над анодными заземлителями в системах катодной защиты, в которых имеется высокая плотность защитного тока и большой градиент потенциалов в грунте. Поскольку при этом происходит смещение потенциалов только в отрицательную сторону, опасности анодной коррозии не возникает. Однако в коррозионных системах группы II ( см. раздел 2.4), например для алюминия и свинца в грунте, все же может произойти катодная коррозия. [40]
Одной из причин роста токоотводов служит разбухание активной массы в процессе эксплуатации аккумулятора. Другой причиной может служить образование оксидной пленки на поверхности металла в результате его анодной коррозии. Удельный объем пленки диоксида свинца зачительно превосходит удельный объем металла, из которого она образуется. Вследствие этого возникает давление на поверхность металла, которое может вызвать появление растягивающих усилий, приводящих к деформации свинцового сплава. [41]
До сих пор еще имеется неопределенность в отношении того, каким образом сульфиды ускоряют коррозию железа в кислотах. Возможно, что адсорбция сероводорода может так изменить электрическое поле на поверхности, что это способствует удалению положительных ионов железа и анодной коррозии при значении потенциала, более близком к обратимым значениям. Хор указывает, что сероводород стимулирует только анодную реакцию и несколько задерживает катодную. [42]
 |
Физико-химические свойства кристаллических модификаций двуокиси свинца. [43] |
В порах анодной пленки происходит непосредственное окисление свинца молекулами воды. Очевидно, реакция окисления металлического свинца водой, выражаемая суммарным уравнением ( 84), играет весьма существенную роль в кинетике анодной коррозии свинца. [44]
Возможность протекания реакции доказана Ландером непосредственными опытами. Однако, как подчеркивает сам автор, указанный процесс, по-видимому, не может играть существенной роли, о чем, в частности, свидетельствует значительное влияние температуры и концентрации кислоты на скорость анодной коррозии свинца. [45]
Страницы: 1 2 3 4