Влажная коррозия
Cтраница 1
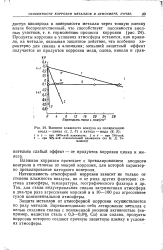 |
Влияние влажности воздуха на поляризацию анода-цинка ( /, 2, 3 и катода - меди ( 4, 5. [1] |
Влажная коррозия протекает с превалированием анодного контроля в отличие от мокрой коррозии, для которой характерно превалирование катодного контроля. [2]
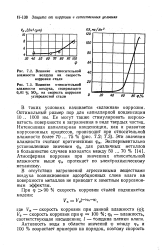
Для влажной коррозии особое значение имеет толщина слоя воды на поверхности; это наглядно демонстрирует рис. 5.43. В области I, где толщина сдоя мрлекул воды меньше цли близка к трлщине мономолекулярного рлоя, коррозия очень незначительна. Обычно при отно-ситедьной цлажности атмосферы 50 - 70 % большинство метадлов почти не подвержено коррозии. Однако в области П, где трлщина рлоя воды составляет нескрлько десятков цли сотен мрлекул, в обычных атмосферных урловиях коррозии подвержены почти все металлы. С увеличением толщины пленки воды и переходом в область III диффузия кирлорода затрудняется и становится лимитирующей стадией процесса, чем и объясняется некоторое уменьшение скорости коррозии в этой области. Область IV соответствует своеобразному погружению метадла в воду, и в этом состоянии, естественно, скорость коррозии перестает зависеть от толщины цленки воды. Все описанные области наблюдаются в действительности, и им соответствуют специфические процессы коррозии, которые принято называть сухой атмосферной коррозией ( область. [4]
При влажной коррозии толщина пленки составляет примерно до 0 1 мкм и при мокрой коррозии - от 0 1 до 1 мкм, такая коррозия протекает по электрохимическому механизму с катодной реакцией восстановления кислорода. [5]
Изучение влажной коррозии железа методом меченых атомов показало, что вначале окисление железа идет за счет меченого кислорода воды. В присутствии солей коррозия ускоряется в ряду СЮГ F - SO4 - Г Вг - СГ. [6]
Чтобы предотвратить влажную коррозию, нужна гораздо более совершенная пленка, чем для предотвращения сухого тускнения. Верной полагает, что предохранение от затуманивания при помощи длительного воздействия неподвижного воздуха при обычной температуре является следствием не образования защитной окисной пленки, а результатом отравления каталитически активных мест на поверхности никеля каким-то антикатализатором, возможно, сероводородом. Это предположение подкрепляется опытами, которые показывают, что воздух, очищенный пропусканием над гранулированным серебром, не дает такого иммунитета. [7]
Для изучения механизма влажной коррозии металлов был применен тяжелый изотоп кислорода. В длительных опытах происходит вторичный обмен кислорода между продуктами коррозии и водой, что сильно затрудняет толкование результатов. [8]
 |
Влияние относительной.| Влияние относительной. [9] |
В таких условиях начинается влажная коррозия. Ее могут также стимулировать шероховатость поверхности и загрязнения в виде твердых частиц. Атмосферная коррозия при значениях относительной влажности выше рк протекает по электрохимическому механизму. [10]
Более подробное количественное исследование влажной коррозии железа в разбавленных растворах MgQ2 выполнили А. С. Фоменко, Т. М. Абрамова и автор 11263 ], применив масс-спектрометрическую методику для изотопного анализа воды, кислорода и продуктов коррозии. Это позволило вести опыты короткое время ( несколько часов), что устраняло осложнения из-за вторичного обмена. [11]
Процесс окисления железа аналогичен процессу влажной коррозии его в присутствии электролитов. В связи с тем, что Fe ( OH) 2 и 2 ато на водорода реакции I немедленно вступают в быстротекущие реакции П и Ш, окисление железа происходит значительно быстрее, чей на влажном воздухе. Для восстановления применяются мягкие, богатые ферритом, перлитом и графитом серые чугуны. Большое значение на скорость процесса восстановления имеет степень дробления стружки, природа электролита, концентрация его и рН среды. [12]
Различные электролиты в разной степени способствуют влажной коррозии железа и потому скорость восстановления зависит не только от концентрации, но и от природы электролита. По данным В. О. Лукашевича, скорость восстановления наиболее высока в присутствии хлористого аммония, затем следует хлористое железо, сернокислый аммоний. Применение хлористого аммония позволяет в ряде случаев получить более высокие выходы, чем в присутствии других электролитов, В процессе восстановления количество электролита в растворе убывает, что объясняется адсорбцией его образующимся осадком окислов железа. [13]
Различные электролиты в разной степени способствуют влажной коррозии железа и потому скорость восстановления зависит не только от концентрации, но и от природы электролита. По данным В. О. Лукашевича, скорость восстановления наиболее высока в присутствии хлористого аммония, затем следует хлористое железо, сернокислый аммоний. Применение хлористого аммония позволяет в ряде случаев получить более высокие выходы, чем в присутствии других электролитов. В процессе восстановления количество электролита в растворе убывает, что объясняется адсорбцией его образующимся осадком окислов железа. [14]
 |
Зависимость скорости коррозии К от толщины б слоя влаги на поверхности металла. / - сухая коррозия. / / - влажная коррозия. / / / - мокрая коррозия. IV - коррозия при полном погружении. [15] |
Страницы: 1 2 3