Восстановленный кофермент
Cтраница 1
Восстановленный кофермент ФАДНд окисляется далее кис, родом с образованием пероксида водорода и регенерат кофермента ФАД. [1]
Для окисления восстановленных коферментов был предложен ряд электродов. [2]
При обратной реакции - ферментативном окислении восстановленного кофермента ацетальдегидом - кофермент полностью освобождается от дейтерия. В противоположность этому при химическом окислении в коферменте сохраняется примерно половина метки. Положение 4 в восстановленном коферменте асимметрично. Приведена формула одного из двух возможных 4-эпимеров. [3]
При обратной реакции - ферментативном окислении восстановленного кофермента ацетальдегидом - кофермент полностью освобождается от дейтерия. В противоположность этому при химическом окислении в коферменте сохраняется примерно половина метки. Положение 4 в восстановленном коферменте асимметрично. Приведена формула одного из двух возможных 4-эпимеров. [4]
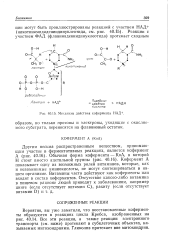 |
Механизм действия кофермента НАД. [5] |
Вероятно, вы уже заметили, что восстановленные коферменты образуются в реакциях цикла Кребса, изображенных на рис. 40.14. Все эти реакции, а также реакции электронного транспорта ( см. ниже) протекают в субклеточных объектах, называемых митохондриями. Гликолиз протекает вне митохондрии. [6]
Однако если для восстановления кофермента I использовать 1-дейтероглкжозу и дегидрогеназу глюкозы, то образующийся дейтерированный восстановленный кофермент может передавать пировиноградной кислоте водород, а не дейтерий. Очевидно, в восстановленном веществе XX связи С - Н и С-D стереохими-чески не эквивалентны, и активирующий фермент должен контролировать направление, по которому спирт или кетон взаимодействует с никотинамидной группой. [7]
Инкубация тимидиндифосфоглюкозы с экстрактами из клеток Pseudotnonas aeruginosa, разрушенных ультразвуком, в отсутствие восстановленного кофермента II ( но в присутствии кофермента I) приводит к получению соединения, являющегося, по-видимому, тимидиндифосфо-4 - кето-6 - дезоксиглюкозой. [8]
Непрерывная работа цикла трикарбоновых кислот или его части требует присутствия соответствующего акцептора водорода для ре-окисления восстановленных коферментов. В отсутствие кислорода как конечного акцептора электронов катализаторы дыхательной цепи находятся в восстановленном состоянии и поэтому не могут служить акцепторами электронов от восстановленных пиридиннуклеотидов и флавинов. В этих условиях акцепторами электронов могут служить другие метаболиты. [9]
Имеются пять окислительных стадий, в результате которых при окислении пирувата до С02 и воды образуются восстановленные коферменты: 1) окисление пирувата до ацетил - КоА и С02; 2) окисление изоцитрата с образованием а-кетоглутарата и С02; 3) окисление а-кетоглутарата до сукцинил - КоА и С02; 4) окисление сукцината до фумарата; 5) окисление малата до оксалоацетата. [10]
Необходимо подчеркнуть, кроме того, что роль цикла Кребса вовсе не ограничивается тем, чтобы поставлять восстановленные коферменты, способные вновь окисляться в цепи реакций, сопряженных с фосфорилиро-ванием. Прежде всего восстановленные кофакторы используются также для восстановления двойных связей, карбонильных групп, имидов и в других восстановительных реакциях, необходимых для синтеза веществ, из которых состоит клетка. Более того, цикл трикарбоновых кислот сам служит источником углеродных скелетов для различных синтезов. У микроорганизмов, растущих на соединениях, состоящих из двух атомов углерода, единственным источником четырех - и пятиуглеродных скелетов, необходимых для синтеза клеточного материала, является совместное функционирование глиоксилатного цикла и цикла трикарбоновых кислот ( фиг. Наконец, в цикле Кребса происходит также сжигание избытка углеродных скелетов, образующихся при деградации определенных аминокислот. [11]
Необходимо еще раз подчеркнуть, что для аэробных организмов эти пять ферментов ( или ферментных систем) служат основным источником восстановленных коферментов, необходимых как для химических синтезов, так и для образования электронов с высоким потенциалом, используемых цитохромнои системой переноса электронов. Окисление этих восстановленных коферментов сопровождается окислительным фосфорилированием. [12]
Стикленда в качестве переносчика водорода участвует дифосфопиридиннуклеотид [187, 188]; так, установлено, что дифосфопиридиннуклеотид может быть восстановлен аланином, а восстановленный кофермент вновь переводится в окисленную форму пролином или глицином. Исследования, проведенные в последние годы, свидетельствуют о том, что процесс сопряженного окислительного и восстановительного дез-аминирования, описанный Стиклендом, состоит из сложного ряда промежуточных реакций; некоторые стороны этого процесса, например природа систем, участвующих в переносе водорода, нуждаются в дальнейшем изучении. [13]
Выше уже упоминался один из коферментов - никотинамидаде-ниндинуклеотид ( НАД), который в сочетании с ферментом алко-гольдегидрогеназой ( АДГ) окисляет этанол в ацетальдегид с образованием восстановленного кофермента ( НАД-Н) и ацетальдеги-да ( 1, разд. [14]
Аналогичным образом ведет себя и кофермент А ( Басфорд и Хкшпекенс); применяя 70 % - ный водный раствор этанола, можно выделить четыре формы: fif 0 42 - восстановленный кофермент A, Rf 0 35 - очевидно, тиазолиновая форма, Rf 0 15 и 0 00 - дисульфиды. [15]
Страницы: 1 2 3