Восстановленный кофермент
Cтраница 2
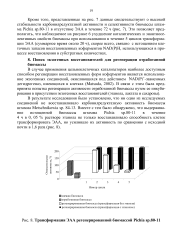 |
Трансформация ЭАА регенерированной биомассой Pichia sp. 80 - 11. [16] |
Это позволяет предполагать, что наблюдаемое на рисунке 6 ухудшение каталитических и энантиосе-лективных свойств биомассы при использовании в течение 5 циклов трансформации ЭАА ( суммарное время около 20 ч), скорее всего, связано с истощением клеточных запасов восстановленных коферментов NAD ( P) H, использующихся в процессе восстановления в субстратных количествах. [17]
Выберите утверждения, правильно характеризующие пенто-зофосфатный путь превращения глюкозы: 1) активно протекает в жировой ткани; 2) включает совместное протекание окислительного пути синтеза пентоз и неокислительного пути превращения их в гексозы; 3) промежуточные продукты могут включаться в специфический путь превращения глюкозы; 4) протекают реакции, сопряженные с ЦПЭ и образованием энергии; 5) образуются восстановленные коферменты, водород которых используется для восстановительных синтезов; 6) образуются пентозы, используемые для синтеза фос-форибозилпирофосфата и нуклеотидов. [18]
Необходимо еще раз подчеркнуть, что для аэробных организмов эти пять ферментов ( или ферментных систем) служат основным источником восстановленных коферментов, необходимых как для химических синтезов, так и для образования электронов с высоким потенциалом, используемых цитохромнои системой переноса электронов. Окисление этих восстановленных коферментов сопровождается окислительным фосфорилированием. [19]
В цитохромах с и Cj дополнительные ковалентные связи формируются между тиогруппами цистеина и боковыми винильными группами тема. Этот фермент катализирует окисление восстановленного кофермента Q и перенос электронов на цитохром с. Электроны последовательно переносятся атомами железа цитохромов Ъ и Cj, а затем поступают на цитохром с. Протоны после окисления QH2 освобождаются в раствор. [20]
В ходе реакций, связанных с дыханием, углеводы, жиры и белки разлагаются до пировиноградной или уксусной кислоты и затем в форме ацетил - КоА включаются в гликозилатный цикл и цикл трикарбоновых кислот, в процессе которого ацетил отщепляется от кофермента А. Для поддержания непрерывности метаболических процессов восстановленные коферменты и молекулы НАД-Н должны окисляться до НАД и воды. [21]
Многие метаболические превращения, как показано на схеме, протекают с участием промежуточного соединения - ацетилкофермента А, который включается в цикл трикарбоно-вых кислот. Образующийся в результате этого цикла восстановленный кофермент НАД-Н2 ( никотинамидадениндинукле-отид) вновь окисляется в цепи реакций так называемого терминального окисления, о котором речь будет дальше, а эти реакции в свою очередь приводят к восстановлению кислорода до воды. [22]
В изолированных митохондриях и в субмитохондриальных частицах, содержащих неповрежденную внутреннюю мембрану, при окислении каждой молекулы NAD-H кислородом в нормальных физиологических условиях образуются три молекулы АТФ, а при окислении одной молекулы сукцината - две молекулы АТФ. Одна молекула АТФ образуется при переносе пары электронов от восстановленного кофермента Q на феррицитохром с, т.е. при прохождении пары электронов через комплекс III, и еще одна молекула - при переносе пары электронов от двух молекул ферроцитохрома с к 0; в комплексе IV. Таким образом, источником энергии для осуществления окислительного фосфорилирования являются реакции ( VIII. [23]
Обратимое окисление - восстановление как механизм, обеспечивающий низкоэнергетический путь каталитической реакции, наблюдается в некоторых ферментативных реакциях, однако при этом обычно не происходит непосредственной активации уходящей группы. После прибавления к ферменту субстрата появляется полоса поглощения при 345 нм, характерная для восстановленного кофермента. [24]
Эти коферменты, как правило, легко отщепляются от соответствующих апоферментов. Восстановленные коферменты часто бывают связаны с белком более прочно, чем окисленные. Ионы Zna могут участвовать в связывании кофермента с белком, как это было доказано для нескольких высокоочищенных дегидрогеназ. Взаимодействие фермента с субстратами во многих случаях происходит при участии тиоловых групп. [25]
Оксидоредуктазы катализируют реакции окисления - восстановления. Окисление заключается в потере атома водорода веществом или во взаимодействии вещества с кислородом. Восстановленные коферменты передают электроны цитохромным системам, которые затем при участии оксидаз окисляются кислородом воздуха. [26]
Никотинамиднуклеотидные ферменты катализируют перенос двух вос-станавительных эквивалентов от субстрата к коферменту, который, как правило, представляет собой легко диссоциирующий переносчик. Именно этим обусловлена их роль катализаторов начальной реакции в цепи переноса электронов - реакции дегидрирования субстрата. Образовавшийся в результате восстановленный кофермент способен далее взаимодействовать с активным центром другого фермента; при этом он может быть использован либо для восстановления второго субстрата, либо в процессах восстановления, необходимых для протекания биосинтетических процессов, либо, наконец, он может быть окислен дыхательной цепью, что сопровождается превращением АДФ в АТФ. [27]
В другом эпимере дейтерий находится над плоскостью рисунка, водород - под ней. Асимметрия невозможна в отсутствие амидной группы. При химическом окислении восстановленного кофермента продукт содержит примерно половину первоначального количества дейтерия. В противоположность этому в результате ферментативного восстановления образуется один специфический эпимер. Дейтерий ( или водород в общем случае) переносится только на одну сторону пиримидинового цикла, что схематически показано на формуле. [28]
При обратной реакции - ферментативном окислении восстановленного кофермента ацетальдегидом - кофермент полностью освобождается от дейтерия. В противоположность этому при химическом окислении в коферменте сохраняется примерно половина метки. Положение 4 в восстановленном коферменте асимметрично. Приведена формула одного из двух возможных 4-эпимеров. [29]
При обратной реакции - ферментативном окислении восстановленного кофермента ацетальдегидом - кофермент полностью освобождается от дейтерия. В противоположность этому при химическом окислении в коферменте сохраняется примерно половина метки. Положение 4 в восстановленном коферменте асимметрично. Приведена формула одного из двух возможных 4-эпимеров. [30]
Страницы: 1 2 3