Коэффициент - пересыщение
Cтраница 2
Значения величины п в тех случаях, когда используются зависимости т от концентрации или коэффициента пересыщения, колеблются в более широких пределах. Различия в значениях порядков процесса кристаллизации связаны с различием физической сущности п при переходе от одной зависимости к другой. [16]
Степень пересыщения может характеризоваться различными величинами: абсолютным или относительным пересыщением, а также коэффициентом пересыщения. Первая из них зависит от способа выражения концентраций, а вторая и третья безразмерны. [17]
Как видим, уравнения ( 46) и ( 44) имеют один и тот же вид, но при небольших пересыщениях раствора время кристаллизации связано не с коэффициентом пересыщения, а с квадратом этой величины. Если поверхность растущих кристаллов претерпевает значительные изменения, ее нужно рассматривать как функцию пересыщения. [18]
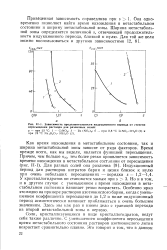 |
Зависимость продолжительности индукционного периода от степени пересыщения раствора для различных солей. [19] |
Соли, кристаллизующиеся в виде кристаллогидратов, ведут себя также различно. С уменьшением коэффициента пересыщения время метастабильного состояния растворов азотнокислого лития возрастает сравнительно плавно. [20]
 |
Зависимость индукционного периода от пересыщения для растворов различных солей при 20 С. [21] |
Так, при измене-всего на 10 - 15 % время на-состоянии растворов Са ( Н2Р04) 2, для которого / г16, изменяется в 15 раз. Изменение же коэффициента пересыщения раствора тетраборнокислого натрия на те же 15 % приводит к изменению величины индукционного периода всего в 2 - 2.5 раза. В первой из них собраны данные, относящиеся в основном к кристаллизации из перемешиваемых растворов. [22]
Время нахождения раствора в метастабильном состоянии зависит от температуры более четко. При одном и том же коэффициенте пересыщения продолжительность индукционного периода с ростом Т уменьшается. Так, при s 1 3 время нахождения растворов азотнокислого бария в метастабильном состоянии при 0 8; 25 и 40 С соответственно равно 90; 23 и 5 мин. Однако, говоря о влиянии температуры, нужно учитывать, что один и тот же коэффициент пересыщения при различных температурах отвечает различным положениям раствора в метастабильной области. [23]
Согласно существующей теории, кристаллизация может происходить из подкачиваемого и межкристального растворов. Важно только, чтобы при помощи теплообмена поддерживался коэффициент пересыщения на оптимальном уровне. Из связи между теплообменом и кристаллизацией следует, что кристаллизация кдет только из подкачиваемого раствора. [24]
При более высокой концентрации сульфат кальция выпадает в осадок, поэтому при нейтрализации сильных кислот, кальциевые соли которых труднорастворимы в воде, необходимо устраивать отстойники-шламонакопители. Существенным недостатком метода нейтрализации серной кислоты известью является также образование пересыщенного раствора гипса ( коэффициент пересыщения может достигать 4 - 6), выделение которого из сточной воды может продолжаться несколько суток, что приводит к зарастанию трубопроводов и аппаратуры. Присутствие в сточных водах многих химических производств высокомолекулярных органических соединений усиливает устойчивость пересыщенных растворов гипса, поскольку эти соединения сорбируются на гранях кристаллов сульфата кальция и препятствуют их дальнейшему росту. [25]
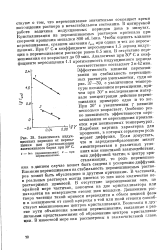 |
Зависимость индукционных периодов от пересыщения для кристаллизации азотнокислого бария при 30 С. [26] |
В цитируемой работе величина индукционных периодов дана в минутах. Кристаллизация из перемешиваемых растворов протекала при скорости вращения мешалки 800 об. / мин. При 0 С и коэффициенте пересыщения 1.5 период индукции в перемешиваемом растворе равен 0.5 мин. В отсутствие перемешивания он возрастает до 69 мин. [27]
Перемешивание пересыщенного раствора, как правило, снижает его устойчивость. При одном и том же коэффициенте пересыщения s - 1 5 и О С в отсутствие перемешивания раствор азотнокислого бария остается без изменения около 70 мин, а в условиях интенсивного перемешивания ( 800 об / мин) - всего 0 5 мин. [28]
Изучение медленной кристаллизации карбоната кальция показало [13], что для начальной стадии осаждения характерен гетерогенный механизм зародышеобразования. Подобная картина наблюдается при низких пересыщениях. При увеличении s, начиная с некоторого критического значения коэффициента пересыщения, становится возможным гомогенное зародышеобразова-ние. Степень пересыщения, при которой начинается фазовое превращение, регулируется скоростью сливания реагентов. В случае гомогенного зародышеобразования сохраняются те же зависимости, но п 1 8 и 0 6 соответственно. [29]
Зависимость скорости роста от пересыщения или переохлаждения может иметь различный вид. Во-первых, это определяется механизмом роста кристалла, а во-вторых, способом выражения пересыщения. Здесь имеется в виду способ выражения степени отклонения системы от состояния равновесия: абсолютное или относительное пересыщение или коэффициент пересыщения. [30]
Страницы: 1 2 3