Коэффициент - погашение
Cтраница 2
Коэффициенты погашения определяют из нескольких исходных навесок. [16]
Коэффициент погашения при данной длине волны и данной температуре раствора является величиной, характерной для каждого химического вещества. Как видно из формулы ( 47 2), при заданном / и з ( л) по измеряемой величине D можно определить концентрацию вещества С. [17]
Коэффициент погашения е называют молярным коэффициентом погашения, если концентрация вещества выражена в моль / л, а толщина слоя - в сантиметрах. [18]
Коэффициент погашения для различных соединений колеблется в пределах 30 - 45 моль-1 л см-1. Она обусловлена колебаниями группы ОН в комплексе с водородной связью ОН-О. Интенсивность этой полосы растет с увеличением концентрации спирта, а интенсивность первой полосы падает. [19]
Коэффициент погашения k зависит лишь от природы растворенного вещества и длины волны падающего света. [20]
Коэффициент погашения зависит также от растворителя, в котором растворено данное вещество. [21]
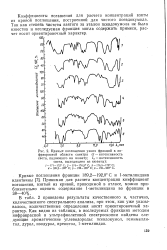 |
Кривые поглощения узких фракций в инфракрасной области спектра ( / - интенсивность света, падающего на кювету. / q - интенсивность света, выходящего из кюветы. [22] |
Коэффициенты погашения для расчета концентраций взяты из кривой поглощения, построенной для чистого псевдокумола. Так как степень чистоты взятого за эталон псевдокумола не была известна и исследуемая фракция могла содержать примеси, расчет носит ориентировочный характер. [23]
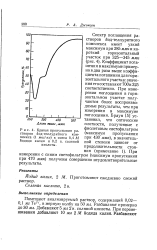 |
Кривая пропускания растворов йод-теллуритного комплекса ( 1 мкг / мл в смеси 0 4 М йодида калия и 0 2 н. соляной кислоты. [24] |
Коэффициент погашения в максимуме примерно в два раза выше коэффициента погашениядля горизонтального участка: значения его составляют 700 и 325 соответственно. При измерении поглощения в горизонтальном участке получаются более воспроизводимые результаты, чем при измерении в максимуме поглощения. [25]
Коэффициент погашения иона Fe3 1 при 365 ту - достаточно велик, а для иона Fe2 равен нулю, поэтому реакция Fe3 Сг2 Fe2 Сг3 пригодна для титрования в ультрафиолетовых лучах. К определенному объему титрованного раствора соли двухвалентного хрома прибавляют большую часть анализируемого на железо раствора при комнатной температуре без перемешивания, затем раствор нагревают и продолжают титровать раствором соли железа до точки эквивалентности. Изменение концентрации НС1 от 0 1 до 2 мол / л не влияет на результаты. [26]
Коэффициент погашения кислот значительно выше коэффициента погашения кетонов, что сильно снижает точность анализа при больших концентрациях кислот. В этих случаях необходимо удалять кислоты из смеси. [27]
Коэффициент погашения рассматриваемой полосы измерялся многими исследователями, и хотя трудно сравнивать значения, полученные на различных приборах, из этих измерений видно, что он имеет довольно постоянное значение. Поскольку данная полоса находится в той спектральной области, в которой обнаруживаются также многие другие колебания, то ее отсутствие можно рассматривать как доказательство отсутствия связи указанного типа; с другой стороны, если эта полоса имеется, необходимо искать другие подтверждения наличия двойной связи путем измерения интенсивности и путем использования других спектральных областей, например областей валентных колебаний С - Н и С С. [28]
Коэффициент погашения рассматриваемой полосы измерялся многими исследователями, и, хотя сравнивать значения, полученные на различных приборах, затруднительно, вполне очевидно, что он имеет довольно постоянную величину. [29]
Коэффициенты погашения йодных комплексов тиофенов и дисульфидов весьма малы по сравнению с коэффициентами погашения комплексов сульфидов. [30]
Страницы: 1 2 3 4