Коэффициент - распределение
Cтраница 1
Коэффициент распределения зависит от температуры, от природы исходной смеси и растворителя, от концентрации извлекаемого компонента и не является величиной постоянной. Поэтому необходимы опытные данные для условий равновесия в различных системах. [1]
 |
Проведение восхс ящей хроматографии иа бумаге. [2] |
Коэффициент распределения для каждого соединения является характерной величиной. [3]
Коэффициент распределения определяет скорость перемещения веществ по слою сорбента. Из уравнения Нернста следует, что изотермы распределения теоретически линейны. Поскольку изотерма, отвечающая уравнению Нернста, линейна, распределение вещества на хроматограмме описывается кривой Гаусса. Скорость перемещения вещества при хроматографическом разделении является величиной характеристической для этого вещества и в данных условиях постоянной. Скорость перемещения оценивают величиной Ry. Величина RF данного вещества представляет собой отношение расстояния от стартовой линии хроматограммы до центра пятна этого вещества в любой момент времени к расстоянию, пройденному за то же время фронтом растворителя. [4]
Коэффициент распределения имеет постоянную величину только для идеальных растворов. В реальных системах, где растворение обычно сопровождается ассоциацией, диссоциацией, ком-плексообразованием, он зависит от концентрации растворенного вещества. [5]
 |
Связь между абсолютным и приведенным времена и удерживания. [6] |
Коэффициент распределения - термодинамическая величина; при определенной температуре колонки каждое вещество характеризуется постоянным коэффициентом распределения. [7]
Коэффициенты распределения применяются в тех случаях, когда требуется определить, какую часть тот или иной абсолютный показатель финансового состояния составляет от итога включающей его группы абсолютных показателей. [8]
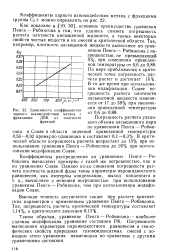 |
Зависимость коэффициентов парного взаимодействия метана с фракциями ДБК от фракций. [9] |
Коэффициенты распределения по уравнению Пенга - Ро - - бинсона вычисляют примерно с такой же погрешностью, как и по уравнению Соаве. Пенга - - Робинсона, чем при использовании модификации Соаве. [10]
Коэффициент распределения можно изменить в ту сторону, в которую облегчается разделение слоев и уменьшается потеря растворителя за счет растворения его в воде. [11]
Коэффициенты распределения, определяемые по графикам фирмы Келлог [22], ложились на сглаженную кривую IgK - bi, за исключением небольшого числа незначительных отклонений, которые, по-видимому, объяснялись случайными ошибками на графиках. [12]
Коэффициент распределения, определяемый по графикам фирмы Келлог, приближается по точности к значениям К, рассчитываемым непосредственно из уравнений Бенедикта [7], и представляет лучший из известных до сих пор способов расчета равновесия жидкость - пар в углеводородных системах. [13]
Коэффициенты распределения, определяемые по графикам Р - Т - Аг, сравнивались с экспериментальными значениями К, полученными автором, а также приводимыми в литературе, перечисленной в табл. 3, за исключением данных для системы метан - этилен - этан. При сравнении не использовались данные для двойных смесей вследствие того, что данные, использованные для построения графиков Кел-лога, были рассчитаны по уравнению Бенедикта для двойных систем и было желательно проворить применимость диаграмм Р - Т - N к сложным системам. [14]
Коэффициенты распределения, снимаемые со сглаженной кривой lg К - bi, проведенной через точки для других углеводородов, имеют ту же степень точности, как и значение IgK, определяемое по графикам. [15]
Страницы: 1 2 3 4