Коэффициент - активность - зависенок
Cтраница 1
Коэффициенты активности зависят от состава жидкости, ее свойств, температуры и давления в системе и вычисляются либо на основе экспериментальных данных, либо по ряду эмпирических уравнений. [1]
Коэффициенты активности зависят от свойств и температуры системы и от состава жидкости. Величина коэффициентов активности либо определяется на основе экспериментальных данных, либо вычисляется при помощи ряда приближенных уравнений. [2]
 |
Вид графиков t - х, у и у - х для реальных растворов жидкостей с неограниченной взаимной растворимостью различных типов. [3] |
Коэффициенты активностей Y зависят от температуры и состава системы и природы компонентов и могут быть подсчи таны по одной или нескольким известным экспериментальным точкам. Однако уравнения для вычисления Yi по отдельным опытным точкам являются приближенными, а в случае многокомпонентной смеси к тому же и весьма громоздкими. Поэтому чаще всего приходится пользоваться даже для двухкомпонентных растворов экспериментальными данными. [4]
Поскольку коэффициенты активности зависят от ряда свойств среды ( диэлектрической проницаемости, заряда частиц, их размеров и химической природы), уравнение ( 6) позволяет найти зависимость скорости реакции от всех этих факторов. [5]
Поскольку коэффициенты активности зависят от ряда свойств среды ( диэлектрической проницаемости, заряда частиц, их размеров и химической природы), уравнение ( 6) позволяет найти зависимость скорости реакции от всех этих факторов. Так как в газовой фазе при не слишком больших давлениях в разбавленных растворах в реакциях между заряженными частицами коэффициенты активностей близки к единице, уравнение Бренстеда - Бьеррума имеет наибольшее значение при объяснении реакций с участием ионов в неразбавленных растворах. [6]
Поскольку коэффициенты активности зависят от ряда свойств среды: диэлектрической постоянной, заряда частиц, их размеров, химической природы и др., это уравнение позволяет вообще говоря найти зависимость от всех этих факторов. [7]
Поскольку коэффициенты активности зависят от ряда свойств среды ( диэлектрической проницаемости, заряда частиц, их размеров и химической природы), уравнение ( 6) позволяет найти зависимость скорости реакции от всех этих факторов. Так как в газовой фазе при не слишком больших давлениях в разбавленных растворах в реакциях между заряженными частицами коэффициенты активностей близки к единице, уравнение Бренстеда - Бьеррума имеет наибольшее значение при объяснении реакций с участием ионов в неразбавленных растворах. [8]
Поэтому коэффициенты активности зависят как от температуры, так и от состава, и температурную зависимость коэффициентов активности можно считать слабо выраженной по сравнению с зависимостью давлений паров чистых жидкостей от температуры. [9]
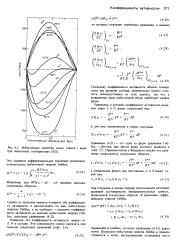 |
Избыточные свойства смеси этанол вода при нескольких температурах. [10] |
Очевидно, что коэффициенты активности зависят от Т, Р я состава. [11]
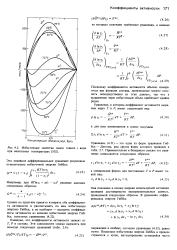 |
Избыточные свойства смеси этанол вода при нескольких температурах. [12] |
Очевидно, что коэффициенты активности зависят от Т, Р я состава. [13]
Но эта зависимость является приближенной, поскольку коэффициенты активности зависят от концентрации. [14]
Из всего сказанного о влиянии междуионных сил следует, что коэффициенты активности зависят не только от концентрации в растворе данного электролита, но и от присутствия в нем других электролитов. Именно, значения коэффициентов активности понижаются с возрастанием так называемой тонной силы раствора, зависящей от концентраций и зарядов всех присутствующих в растворе ионов. [15]
Страницы: 1 2