Коэффициент - активность - неэлектролит
Cтраница 1
 |
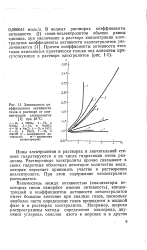
Зависимость коэффициента активности тростникового сахара ( / и хлорида лития ( 2 от их концентрации в водном растворе. [1] |
Коэффициент активности неэлектролита растет с ростом концентрации. Для электролитов наблюдается вначале падение Y с ростом т, которое лишь при высоких концентрациях сменяется ростом коэффициента активности. Термодинамический метод, указывая на специфику в поведении растворов электролитов, тем не менее, не может объяснить этих особенностей. Таким образом, возникает необходимость рассмотреть ион - ионное взаимодействие с точки зрения модельных представлений. [2]
Рассмотрим определение этим способом коэффициента активности неэлектролита. [3]
В двойных системах зависимость коэффициента активности неэлектролита от состава смеси обычно достаточно хорошо описывается двучленным уравнением Маргул-еса. Уравнение Маргулеса в его простейшей форме распространено Уолом [5] на тройные системы. [4]
Согласно уравнению ( 2 - 29), логарифм коэффициента активности неэлектролита должен быть пропорционален ионной силе. Если растворяемое вещество имеет более низкую диэлектрическую проницаемость, чем растворитель, что обычно наблюдается в водных растворах, то константа пропорциональности k - величина положительная. [5]
Однако для большинства химико-аналитических расчетов это не имеет существенного значения и коэффициенты активности неэлектролитов обычно принимаются равными единице. Для разбавленных растворов это соблюдается вполне строго. [6]
Благодаря кулоновскому взаимодействию между ионами коэффициенты активности электролитов в разбавленных растворах отличаются от коэффициентов активности неэлектролитов, как показано в теории Дебая-Хюккеля. Эта теория является основой для установления эмпирических соотношений между коэффициентами активности в некоторой области концентраций, включая коэффициенты активности растворов нескольких электролитов. [7]
В то время совсем не было или почти не существовало каких-либо данных по коэффициентам активности неэлектролитов, которые могли бы послужить для проверки этой идеи, и большинство химиков принимало догму, что все реакции между ионами протекают мгновенно. [8]
 |
Зависимость коэффициентов активности газов в растворе от концентрации электролитов при 25 0. [9] |
Взаимосвязь между активностью ( анализаторы некоторых типов измеряют именно активность), концентрацией и коэффициентом активности неэлектролитов имеет большое значение при анализе газов, поскольку наиболее часто определение газов проводится в жидкой фазе и в растворах электролитов. [10]
В общем случае, надо помнить, что с увеличением концентрации электролита в воде возрастает коэффициент активности неэлектролита и с увеличением радиуса катиона растет вса-ливание неэлектролита. Таким образом, для проведения реакции по механизму всаливания необходимо повышать концентрацию длинноцепочечного катиона в водной фазе. [11]
Согласно теории Дебая - Гюккеля, растворы неэлектролитов должны вести себя как идеальные, а коэффициенты активности неэлектролитов должны быть равными единице при любом значении ионной силы. Экспериментально показано, что коэффициенты активности неэлектролитов в растворах меньше отклоняются от единицы, чем коэффициенты активности электролитов. Однако очевидно, что если добавление электролита оказывает высаливающее действие, то коэффициент активности неэлектролита должен возрастать с увеличением ионной силы раствора. Допустим, что Sw - растворимость неэлектролита в воде, больше 5S - его растворимости в растворе соли. В обоих случаях при наличии насыщенного раствора должно существовать равновесие между раствором и твердым веществом; отсюда следует, что активности неэлектролита в этих двух растворах равны. [12]
Однако очевидно, что если добавление электролита оказывает высаливающее действие, растворимость при этом понижается, и коэффициент активности неэлектролита должен возрастать с увеличением ионной силы раствора. Допустим, что Sw - растворимость неэлектролита в воде, больше Ss - его растворимости в растворе соли. В обоих случаях при наличии насыщенного раствора должно существовать равновесие между раствором и твердым веществом; отсюда следует, что активности неэлектролита в этих двух растворах равны. [13]
Коэффициенты активности неэлектролитов и слабых электролитов в водных растворах при всех концентрациях близки к единице. [14]
Нельзя также ожидать, что будут симметричными отношения коэффициентов активности, как это было в разд. Влияние солей на коэффициенты активности неэлектролитов также может быть ощутимым. Поскольку не всегда можно измерить коэффициент активности основания и сопряженной кислоты в сильнокислом растворе, единственная оставшаяся возможность состоит в применении нетермодинамического метода. Этот подход действительно оказался весьма плодотворным. [15]
Страницы: 1 2