Коэффициент - активность - вещество
Cтраница 2
При расчете константы равновесия этой гетерогенной реакции ( константы обмена) следует учитывать коэффициенты активности веществ в растворе и в сорбенте. [16]
Уменьшение скорости реакции с увеличением концентрации кислоты может быть обусловлено происходящими при этом изменениями коэффициентов активности обменивающихся веществ и активированного комплекса. [17]
На основании приведенных ниже данных для системы хлороформ ( А) - ацетон ( В) вычислить коэффициенты активности веществ А и В, а также избыточную мольную свободную энергию раствора как функцию состава. [18]
Этот результат заслушивает внимания, так как, зная BRI, можно по уравнению ( 46) определить коэффициент активности насыщающего вещества в чистой воде из данных о его растворимости в смесях солей при высокой ионной силе. [19]
Этот результат заслуживает внимания, так как, зная Врц, можно по уравнению ( 46) определить коэффициент активности насыщающего вещества в чистой воде из данных о его растворимости в смесях солей при высокой ионной силе. [20]
Другими словами, если энергия взаимодействия между атомами х и у больше, чем между Me и х, то введение вещества х понижает коэффициент активности вещества у, увеличивая ( как это будет показано ниже) растворимость у в Me. Соотношение ( 7), как показывает опыт, имеет место для х Мп, Сг, V, если Me Fe, а у С. [21]
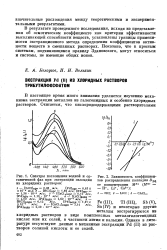 |
Спектры поглощения водной и органической фаз при экстракции палладия из хлоридных растворов.| Зависимость коэффициентов распределения палладия ОрЛ от концентрации Мп ( Мп Н, Li, Са2. [22] |
В результате проведенного исследования, исходя из представления об осмотическом коэффициенте как критерии эффективности высаливающей способности веществ, установлены границы применимости экстракционного метода определения коэффициентов активности веществ в смешанных растворах. Показано, что к простым системам, подчиняющимся правилу Здановского, могут относиться и системы, не имеющие общих ионов. [23]
По Шварценбаху, аналогия заключается в том, что коэффициенты активности YOBH и VOB так же как и коэффициенты активности YOHA и VOA - представляют коэффициенты активности веществ, отличающихся только одним зарядом. [24]
Коэффициент распределения КЕ в общем случае не может быть постоянной величиной, так как его значение определяется составом раствора и является сложной функцией концентраций и коэффициентов активности веществ, участвующих в реакции. [25]
 |
Зависимость формы хромато-графических пиков от вида изотерм адсорбции. Концентрация компонента. [26] |
Могут быть определены термодинамические характеристики адсорбции и растворения, а именно: константы Генри, изменения внутренней энергии, энтропии и теплоемкости при адсорбции, энтальпии и энтропии при растворении; коэффициенты активности вещества в адсорбированном и растворенном состоянии; энергия образования водородной связи, получение изотерм адсорбции и растворения. [27]
Необходимо учитывать, что в методе фазового равновесия вышеприведенное уравнение можно применять для количественных расчетов только в том случае, если величина Kt не зависит от концентрации анализируемого вещества, т.е. для разбавленных растворов, у которых в интервале определяемых концентраций коэффициенты активности веществ должны иметь постоянную величину или быть близки или равны единице. [28]
 |
К определению адсорбционной активности А. [29] |
Следует помнить, что в области высоких концентраций ПАВ в растворе замена адсорбции как избыточной величины общим содержанием вещества в адсорбционном слое недопустима. Кроме того, необходимо учитывать коэффициенты активности вещества в объеме раствора. [30]
Страницы: 1 2 3