Коэффициент - активность - электролит
Cтраница 2
Коэффициенты активности электролитов типа соляной кислоты при концентрациях, значительно превышающих границу так называемой области Дебая-Хюккеля ( т 0 01), представляют с помощью более сложных выражений с одним или более подгоночным параметром. [16]
Зависимость коэффициентов активности электролитов от состава раствора является важной и сложной проблемой физической химии. Для бинарных растворов сильных электролитов существуют удовлетворительные способы описания, основанные на теории Дебая-Хюккеля. Ниже мы попытаемся показать, что обширны экспериментальные данные по смешанным растворам электролитов являются важным полигоном для испытания теорий. [17]
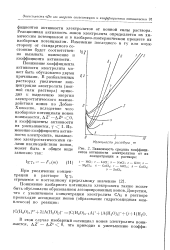 |
Зависимость средних коэффициентов активности электролитов от их концентрации в растворе. [18] |
Понижение коэффициента активности электролита может быть обусловлено двумя причинами. [19]
Определение коэффициентов активности электролитов в смешанных растворах двух электролитов с общим ионом чаще всего производится путем измерения активности растворителя с последующим использованием уравнения Гиббса - Дюгема. [20]
Между коэффициентом активности электролита и ионностью среды растворителя имеется определенная эмпирически установленная взаимосвязь. Коэффициент активности / данного электролита в растворе зависит только от ионности среды раствора. При одинаковом значении / коэффициент активности сохраняет свое постоянное значение независимо от вида остальных электролитов, присутствующих в растворе. Это правило справедливо как для электролита в целом, так и для каждого из составляющих его ионов в отдельности. [21]
Если известен коэффициент активности электролита 1 в чистой воде в интервале достаточно высоких концентраций, необходимых для вычисления Вяь то еГ цо) и а13 могут быть определены с помощью одного опыта по измерению растворимости в чистом растворителе и одного определения растворимости в присутствии второго растворенного вещества. Эти значения коэффициентов активности обычно бывают известны. [22]
Если известен коэффициент активности электролита 1 в чистой воде в интервале достаточно высоких концентраций, необходимых для вычисления 5дь то e i ( o) и ai2 могут быть определены с помощью одного опыта по измерению растворимости в чистом растворителе и одного определения растворимости в присутствии второго растворенного вещества. Эти значения коэффициентов активности обычно бывают известны. [23]
Начаты измерения коэффициентов активности электролитов в других смешанных растворах, что до последнего времени достигалось только применением весьма сложной и кропотливой изопиестической методики. Более полное решение этой задачи может быть достигнуто при создании высокоспецифичных электродных стекол с металлической функцией. [24]
При определении коэффициентов активности электролитов возникают осложнения. [25]
Начаты измерения коэффициентов активности электролитов в других сме-шаннйх растворах, что до последнего времени достигалось то лько применением весьма сложной и кропотливой изопиестической методики. Более полное решение этой задачи может быть достигнуто при создании высокоспецифичных электродных стекол с металлической функцией. [26]
При определении коэффициентов активности электролитов возникают осложнения. [27]
Этим методом определяют коэффициент активности электролита в целом, а не отдельных его ионов. Метод экспериментального определения коэффициентов активности отдельных ионов еще не разработан. Поэтому измеряют коэффициент активности электролита в целом, рассчитывают его активность и затем путем различных допущений оценивают активности ионов. [28]
Обычно при определении коэффициентов активности электролитов экспериментально измеренные активности относятся ко всей брутто концентрации электролита. При таком приеме стандартизации неполная диссоциация сказывается в значительном снижении коэффициентов активности ионов таких электролитов. [29]
Обычно при определении коэффициентов активности электролитов экспериментально измеренные активности относятся ко всей брутто концентрации электролита. При этом неполная диссоциация сказывается в значительном снижении коэффициентов активности ионов таких электролитов. Если отнести экспериментально определенные активности к истинной концентрации ионов, то получаются так называемые ионные коэффициенты активности, величина которых не зависит от степени диссоциации. Подробно эти соотношения рассматриваются в гл. [30]
Страницы: 1 2 3 4