Температурный коэффициент - диффузия
Cтраница 2
Для кинетики гетерогенных процессов в диффузионной области характерны следующие особенности: а) сравнительно малые величины условной энергии активации; б) сравнительно малое влияние температуры на скорость процесса, что видно хотя бы из значений температурных коэффициентов диффузии, которые для жидкостей и газов колеблются в пределах 1 1 - 1 5 ( если только повышение температуры не меняет фазового состояния реагентов); в) большое влияние турбулизацин системы ( перемешивания) на скорость процесса. [16]
Экспериментально определить составляющие энергии Гиббса активации диффузии невозможно, но если допустить, что энтропийный член этой энергии не зависит в первом приближении от температуры, то можно, исходя из общей теплоты активации, рассчитанной по температурному коэффициенту диффузии и теплоте сорбции, определенной из равновесных измерений, вычислить вторую составляющую теплоты активации диффузии, приходящуюся на преодоление механических препятствий, встречающихся на пути движения частицы красителя в волокне. [17]
Большое значение имеет то, что скорость диффузии растворенных атомов в металлах часто бывает велика по сравнению со скоростью растворения газов в металлах или со скоростью десорбции с поверхности металла. Температурный коэффициент диффузии водорода через никель или платину полностью определяется теплотой десорбции с поверхности этих металлов водорода [169], выделяющегося в виде молекул. [18]
Повышение температуры в большинстве случаев является эффективным средством ускорения растворения. Когда процессы растворения подчиняются диффузионной кинетике, температурный коэффициент их скорости практически совпадает с температурным коэффициентом диффузии: при возрастании температуры на 10 К скорость растворения увеличивается в 1 5 - 2 раза. Повышение температуры способствует снижению вязкости раствора и, следовательно, уменьшает толщину диффузионного слоя и его сопротивление массопере-даче - значение К. Для веществ же, растворимость которых с повышением температуры уменьшается, нагревание может не только не ускорить, но даже замедлить или совсем приостановить этот процесс. [19]
Повышение температуры в большинстве случаев является эффективным средством ускорения растворения. Когда процессы растворения подчиняются диффузионной кинетике, температурный коэффициент их скорости практически совпадает с температурным коэффициентом диффузии: при возрастании температуры на 10 К скорость растворения увеличивается в 1 5 - - 2 раза. Повышение температуры способствует снижению вязкости раствора и, следовательно, уменьшению толщины диффузионного слоя и его сопротивления массопередаче - значение К возрастает. Помимо этого при повышении температуры возрастает растворимость х0 большинства веществ и, следовательно, увеличивается движущая сила растворения хп-х, а поэтому и скорость растворения. Для веществ, растворимость которых с повышением температуры уменьшается, нагревание может не только не ускорить, но даже замедлить или совсем приостановить этот процесс. [20]
Повышение температуры является наиболее эффективным средством, ускоряющим процессы растворения и выщелачивания. Так как процессы растворения в основном являются диффузионными, то температурный коэффициент их скорости практически совпадает с температурным коэффициентом диффузии: при повышении температуры на 10 скорость растворения увеличивается в 1 5 - 2 раза. Повышение температуры способствует уменьшению вязкости раствора и, следовательно, уменьшению толщины диффузионного слоя и его сопротивления массопередаче. С другой стороны, при повышении температуры возрастает предельная растворимость большинства веществ хо и, следовательно, увеличивается движущая сила физического растворения хо-х, а поэтому и скорость растворения. [21]
Повышение температуры является наиболее эффективным средством, ускоряющим процессы растворения и выщелачивания. Так как процессы растворения в основном являются диффузионными, то температурный коэффициент их скорости практически совпадает с температурным коэффициентом диффузии: при повышении температуры на 10 скорость растворения увеличивается в 1 5 - 2 раза. Повышение температуры способствует уменьшению вязкости раствора и, следовательно, уменьшению толщины диффузионного слоя и его сопротивления массопередаче. С другой стороны, при повышении температуры возрастает предельная растворимость большинства веществ х0 и, следовательно, увеличивается движущая сила физического растворения Х0 - х, а поэтому и скорость растворения. Для веществ же, растворимость которых с повышением температуры уменьшается, подъем температуры может не только не ускорить, но даже замедлить или совсем приостановить этот процесс. [22]
С возрастанием размера диффундирующих молекул эта зависимость превращается в уравнение Стокса-Эйнштейна. В данной смеси растворителей температурный коэффициент диффузии не зависит от размера диффундирующих молекул и приближенно равен температурному коэффициенту вязкости растворителя. [23]
В интервале давлений 100 - 760 мм происходила кнудсе-новская диффузия наряду с обычной диффузией, вероятно в результате наличия как микро -, так и макропористой структуры. Кривые зависимости коэффициента диффузии от обратной величины общего давления при экстраполяции не проходят через начало координат. Это происходит, вероятно, потому, что при высоких давлениях коэффициент диффузии не становится обратно пропорциональным общему давлению, как того требует классическая теория диффузии, в) Температурный коэффициент диффузии не соответствует ни диффузии Кнудсена, ни обычной диффузии, но увеличивается более быстро в интервале 0 - 200 С. Такие аномальные результаты на активированных углях Вике считает доказательством поверхностной миграции по стенкам поры. Под этим понимается двумерная диффузия на стенках поры в отличие от обычной трехмерной диффузии в пространстве поры. Вике представляет эту диффузию как нечто вроде перескока с одного места адсорбции в другое. По его данным энергия активации равна нескольким килограмм-калориям на моль. [24]
D от ф Кр различен: первая охватывает область низких и средних ф Кр, вторая - область высоких ф кр. При этом D изменяется не пропорционально ф кр и не по прямой в координатах IgD - ф кр, а более сложным образом. Температурный коэффициент диффузии постоянен, а кинетика сорбции - нормальная, фиковская. [25]
Гетерогенные процессы, сопровождаемые химической реакцией, могут быть трех типов: 1) когда реакция протекает на поверхности раздела фаз, этот тип характерен для процессов с участием твердой фазы: Т - Ж; Т - Г; Г - Ж - Т и др.; 2) когда реакции протекают в объеме одной из фаз после переноса в нее вещества из другой; такие процессы наиболее распространены и могут идти с участием любых фаз в системах: Г - Ж, Ж - Ж ( несмешивающиеся), Т - Ж, Г - Ж - Т и др.; 3) когда реакция происходит на поверхности вновь образующейся фазы; этот тип возможен для процессов взаимодействия твердых фаз. Если гетерогенный процесс идет в кинетической области, то для первых двух указанных типов справедливы законы кинетики гомогенных процессов. При этом скорость процесса лимитируется скоростью химических реакций, описывается кинетическими уравнениями реакций, порядок которых зависит от числа и природы реагентов. Для кинетики гетерогенных процессов в диффузионной области характерны следующие особенности: а) сравнительно малые величины условной энергии активации; б) сравнительно малое влияние температуры на скорость процесса, что видно хотя бы из значений температурных коэффициентов диффузии, которые для жидкостей и газов колеблются в пределах 1 1 - 1 5 ( если только повышение температуры не меняет фазового состояния реагентов); в) большое влияние турбулизации системы ( перемешивания) на скорость процесса. [26]
Для зависимости Яп на полярограмме 7 - 10 - 9 М раствора Cd ( II) на фоне 0 1 М КС1 от температуры в интервале от 16 до 45 С ( / - 3 мин, Еп - 0 65 В нас. Такой высокий температурный коэффициент ( температурный коэффициент Яв в классической полярографии составляет около 2 % / К) определяется, в частности, и расширением ртути в резервуаре СРЭ. При объеме резервуара 0 15 см3 и г0 0 04 см температурный коэффициент прироста радиуса капли составляет 3 3 % / К. Авторы [86] однако отмечают, что в этих опы -, тах термостатировали раствор в электролизере с водяной рубашкой, а температура ртути в резервуаре отличалась от температуры раствора. Поэтому основная составляющая температурного коэффициента высоты пика определяется температурными коэффициентами диффузии деполяризатора в растворе и амальгаме. [27]
 |
Энергия активации диффузии воды в пластифицированном. [28] |
Можно видеть, что во всех случаях экспериментальные точки хорошо укладываются на прямые, угол наклона которых и отрезок, отсекаемый на оси ординат, закономерно изменяются с изменением температуры и предыстории образцов. Интересно, что уравнение (4.55) описывает не только высокоэластическое и вязкотекучее состояния пластифицированных систем, но и стеклообразное. Особенность стеклообразного состояния этих систем проявляется в зависимости D от термической предыстории сред. Этот эффект проявляется наиболее ярко для пластифицированного ПВХ в области составов, близких к чистому полимеру. На рис. 4.31 представлены результаты, полученные разными авторами. В области р0 6 коэффициент и плотность матриц связаны линейной зависимостью. Температурный коэффициент диффузии воды в ПВХ в области температур меньших, равных и несколько больших Гс слабо зависит от содержания пластификатора и предыстории образца. Эти результаты близки к опубликованным в работе [243], в которой рассматривалось влияние отжига ПВХ на диффузию и газопроницаемость. [29]
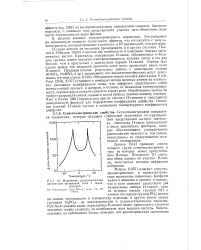 |
Изменение диэлектрической постоянной сегнетовой соли с температурой. [30] |
Страницы: 1 2 3