Концентрационный коэффициент - активность
Cтраница 2
Если растворимости не так малы, то и тогда можно обойтись без определения концентрационных коэффициентов активности, находя для обоих растворителей растворимость при нулевой ионной силе. Для этого определяют растворимость данной соли в присутствии посторонних солей в различных концентрациях. [16]
Упростим нашу задачу: представим, что растворы настолько разбавлены, что отношение концентрационных коэффициентов активности 7в / Твн равно единице. Но и тогда в выражении остается отношение единых коэффициентов активности у0; они не зависят от концентрации. [17]
Отклонения абсолютного коэффициента активности от единицы свидетельствуют о неидеальности раствора, тогда как отклонения концентрационного коэффициента активности от единицы указывают лишь на отклонения от свойств разбавленных растворов. Следует подчеркнуть, что превышение абсолютного коэффициента активности над единицей указывает на положительную неидеальность системы. Например, рост концентрационных коэффициентов активности многих сильных электролитов в водных растворах с увеличением их концентрации отражает отрицательную неидеальность систем и вызван взаимодействием ионов с молекулами воды. [18]
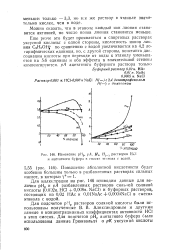 |
Изменение рНр, рА, Н0, Я растворов НС1 и ацетатного буфера в смесях этанола с водой. [19] |
Для подсчетов рНр растворов соляной кислоты были использованы полученные В. В. Александровым и другими данные о концентрационных коэффициентах активности НС1 в этих смесях. [20]
Коэффициенты активности у, отнесенные к бесконечно разбавленному раствору этого вещества в спирте же, являются концентрационными коэффициентами активности. Они характеризуют изменение состояния вещества в данном растворителе в связи с изменением его концентрации. Коэффициенты активности у характеризуют изменение состояния вещества как в связи с изменением концентрации, так и в связи с изменением растворителя. Единые нулевые коэффициенты активности у характеризуют изменения энергии вещества при его переходе от бесконечно разбавленного спиртово - vo раствора к бесконечно разбавленному водному раствору. [21]
Необходимо еще раз подчеркнуть, что, как это следует из уравнения (1.130), распределение воды не влияет на концентрационные коэффициенты активности аммониевых солей до тех пор, пока степень гидратации h постоянна. [22]
Упрощения, использованные в работе [224], по мнению самих авторов, довольно серьезны: применена теория регулярных растворов; не учтены диполь-квадрупольные взаимодействия, которые при исполАзовании сильно полярных разбавителей могут играть существенную роль; принято, что ионизационные потенциалы для всех разбавителей равны; не учтен индукционный эффекту координационные числа и расстояния между взаимодействующими частицами во всех разбавителях приняты одинаковыми; не учтены концентрационные коэффициенты активности. Тот факт, что в ряде случаев получено вполне удовлетворительное согласие теории с опытом, объясняется [224] взаимной компенсацией некоторых из перечисленных противоположно направленных эффектов. Подобное же предположение привлекается Розеном [217] для объяснения близости значений dil при экстракции уранилнитрата системами ТБФ - разбавители. Как отмечает Розен ( [217], стр. ТБФ - разбавитель и соль-ват иО2 ( МО3) 2 2ТБФ - разбавитель, противоположно влияющие на dil), небольшую разницу двух больших величин. Без исследования взаимодействий в бинарных системах нельзя сказать, чем эта разница обусловливается. [23]
Эти же взаимодействия сказываются и на коэффициенте распределения. Предварительно найдем концентрационный коэффициент активности сольвата - уи - За стандартное состояние принимаем раствор сольвата в ТБФ; тогда искомый коэффициент активности принимается равным единице в отсутствие разбавителя ( У. [24]
 |
Зависимость изменения стехиометрической смеси SNa Cl. [25] |
Из табл. 2 следует, что значения у почти не изменяются при замене этиленгликоля глицерином, если суммарная мольная доля неэлектролита в растворе остается постоянной 2увеэл const. С увеличением 2унеэл значения концентрационных коэффициентов активности уменьшаются. [26]
Рассмотрим растворимость малорастворимых солей. Для растворов этих солей величины концентрационных коэффициентов активности у близки к единице. [27]
В нем подробно рассматриваются вопросы зависимости концентрационных коэффициентов активности от гидратации ионов и вопросы подвижности ионов. [28]
Следовательно, для определения jn нужно знать растворимости и т насыщенных растворов. Необходимо иметь в виду, что в уравнение входят не сами концентрационные коэффициенты активности, а их отношение. [29]
Следовательно, для определения YO нужно знать растворимости и 7 насыщенных растворов. Необходимо иметь в виду, что в уравнение входят не сами концентрационные коэффициенты активности, а их отношение. Для малорастворимых солей, таких, как хлористое серебро, концентрационные коэффициенты активности у близки к единице, а их отношения 7в / 7м еще ближе к единице. [30]
Страницы: 1 2 3