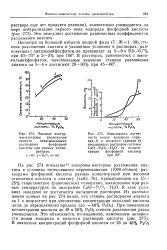
Равновесный коэффициент
Cтраница 1
 |
Формулы для уравнения состояния Соува - Редлиха - Квонга. [1] |
Равновесные коэффициенты рассчитываются по уравнению состояния с использованием одной из зависимостей ( 8) - ( 11), приведенных в § 4.2.1. Все термодинамические величины могут быть связаны друг с другом с помощью математических зависимостей. [2]
Равновесный коэффициент а определяется физико-химическим равновесием в системе. В области малых концентраций примеси он может быть постоянным и не зависеть от содержания других примесей в растворе. В области же больших концентраций он, как правило, зависит от концентрации рассматриваемой примеси и от содержания других примесей в растворе. Коэффициент а зависит также от температуры фракционирования и физико-химических свойств растворителя. [3]
Равновесный коэффициент сегрегации / г0 зависит от природы примесных атомов и предела их растворимости, главным образом в твердой фазе. [4]
Для определения равновесного коэффициента кристаллизации ( D) было проведено несколько опытов ( табл. 2), в которых уран Хг в различных условиях осаждался с мелкокристаллическими осадками оксалата урана. Как показывают опыты 1 - 4 ( табл. 2), постоянные значения D за время около 10 дн. Неполное установление равновесия здесь, очевидно, не связано с какими-либо принципиальными причинами, а объясняется замедленностью перекристаллизации оксалата урана. [5]
 |
Зависимость коэффициента пере. [6] |
Результаты расчета равновесного коэффициента переноса для 750 С показаны на рис. 4 сплошной линией. [7]
В А - равновесный коэффициент сорбции микрокомпонента слоем A; Tj и Г2 - постоянные. [8]
Это замедляет достижение равновесных коэффициентов разложения апатита. [10]
Ранее отмечалось, что равновесные коэффициенты растекания обычно имеют отрицательное значение. Поэтому при нанесении на жидкость А избыточного количества вещества В в равновесных условиях гиббсовский монослой сосуществует с объемной фазой ( или линзой, если В - жидкость), в которой остается избыток В. [11]
Это сильно замедляет достижение равновесного коэффициента разложения апатита. [12]
При этом, однако, равновесный коэффициент k0 заменяется эффективным коэффициентом распределения k, зависящим от степени перемешивания и других условий процесса. [13]
Как отмечается в [7], равновесные коэффициенты растекания обычно имеют отрицательное значение. Поэтому при нанесении на жидкость А избыточного количества вещества В в равновесных условиях гиббсовский монослой сосуществует с объемной фазой ( или линзой, если В - жидкость), в которой остается избыток В. Однако, если А - твердое тело, на поверхности образуются стабильные толстые пленки, т.е. краевой угол равен нулю. Еще одно исключение - стабильное растекание с образованием дуплексных пленок на поверхности раздела вода - масло в присутствии ПАВ. [14]
Сразу бросается в глаза, что хотя равновесные коэффициенты РЕ росли до конца 1986 г. и вновь это имеет склонность ПРОИСХОДИТЬ на рынке быков, они не росли так же быстро, как Чены акций. Другими словами, прибыли компаний и их доходы Ыстро росли, частично оправдывая рост цен на акции. [15]
Страницы: 1 2 3 4