Равновесный коэффициент - распределение
Cтраница 1
Равновесный коэффициент распределения зависит только от природы компонентов. [1]
 |
Зависимости СК / С0 от и ( / и С0 / Ср от Н ( 2 для ионов калия в Nal ( a и примеси КС1 в воде ( б. Пояснения-в подписях под 22 и 23. [2] |
Равновесный коэффициент распределения можно непосредственно рассчитывать по формуле ( 28), если из диаграммы состояния известны наклоны линий ликвидуса и солидуса вблизи ординаты чистого вещества. Пример такого расчета для примеси хлоридов в Nal приведен в разд. [3]
Значение равновесных коэффициентов распределения в области малых концентраций как первого, так и второго компонента позволяет судить о типе диаграммы плавкости исследуемой системы. & oil, а &321 или наоборот, то в этом случае изучаемая система имеет диаграмму плавкости типа, простая сигара. [4]
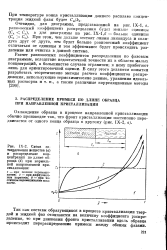 |
Схема затвердевания вещества ( а и распределение концентраций по длине образца ( б при нормальной направленной кристаллизации. [5] |
Расчет равновесных коэффициентов распределения по фазовым диаграммам, вследствие недостаточной точности их в области малых концентраций, в большинстве случаев ограничен; к нему прибегают лишь для ориентировочной оценки. [6]
 |
Уточнение зависимо - рассмотренного случая модель БПС сти, представленной на ни в качественном, ни в количественно. [7] |
Следовательно, равновесный коэффициент распределения очень мал. [8]
Для оценки равновесного коэффициента распределения часто используются следующие эмпирические закономерности: 1) тетраэдри-ческий радиус многих примесей в германии и кремнии при температуре плавления полупроводника изменяется симбатно с изменением коэффициента распределения. Эта зависимость определяется типом вхождения примеси в решетку основного вещества и характером образующихся связей; 2) зависимость между k0 и стандартными энтальпиями сублимации примесей при температуре плавления; основой корреляции - служит зависимость между энергией атомов в простом веществе и твердом растворе его в полупроводниковом материале. [9]
Для оценки равновесного коэффициента распределения часто используются следующие эмпирические закономерности: 1) тетраэдри - ческий радиус многих примесей в германии и кремнии при температуре плавления полупроводника изменяется симбатно с изменением коэффициента распределения. Эта зависимость определяется типом вхождения примеси в решетку основного вещества и характером образующихся связей; 2) зависимость между k0 и стандартными энтальпиями сублимации примесей при температуре плавления; основой корреляции служит зависимость между энергией атомов в простом веществе и твердом растворе его в полупроводниковом материале. [10]
При определении равновесных коэффициентов распределения иногда полезно использовать корреляционные зависимости & о от некоторых физико-химических свойств очищаемого вещества и вещества-примеси. [11]
Различие между эффективным и равновесным коэффициентом распределения заключается в том, что движущийся фронт кристаллизации отталкивает растворенную примесь быстрее, нежели она успевает диффундировать в глубь расплавленной зоны, поэтому впереди фронта кристаллизации возникнет обогащенный слой. Это приводит к тому, что при дальнейшем передвижении зоны содержание примеси в растущих кристаллах повышается но сравнению с равновесными условиями. Толщина а обогащенного слон, обычно называемого диффузионным слоем, лежит в пределах 0 1 - 0 001 см, понижаясь в зависимости от степени интенсивности перемешивании жидкой фазы. Таким образом, диффузионный слой является своеобразной мембраной, препятствующей свободному проникновению примеси в жидкую фазу, и усилия экспериментатора направлены па то, чтобы уменьшить и толщину, и площадь зтой мембраны. [12]
 |
К оценке равновесного коэффициента распределения из диаграммы состояния при fe0 1 ( а и k0 1 ( б. DC-линия ликвидуса. DB-линия солидуса. [13] |
Иначе говоря, равновесный коэффициент распределения равен отношению угловых коэффициентов линий ликвидуса и солидуса. Примеси, понижающие температуру плавления вещества ( рис. 7 а), имеют fc0 1 и, следовательно, оттесняются фронтом кристаллизации в расплав. Примеси, которые увеличивают температуру плавления ( рис. 7 б), имеют k0 1 и перемещаются в направлении, противоположном направлению движения фронта кристаллизации. [14]
Таким образом, макроскопический равновесный коэффициент распределения k0, равный отношению содержаний примеси в соприкасающихся твердой и жидкой фазах в условиях равновесия, может быть выражен через константы скорости процессов ассоциации и диссоциации. [15]
Страницы: 1 2 3 4 5