Стехиометрический коэффициент - реакция
Cтраница 1
Стехиометрический коэффициент реакции быстро изменяется в ходе реакции от 2 до 3, и потому недостаточно только наблюдений за изменением давления, чтобы изучить поведение этой системы. [1]
Стехиометрический коэффициент реакций взаимодействия активного хлора с нитрофенолами в кислой среде составляет в среднем 4 - 6 моль и увеличивается при переходе в нейтральную область до 7 - 8 моль. В ряде случаев небольшое поглощение хлора отмечается и после исчезновения нитрофенолов в реакционной смеси. Для пикриновой кислоты этот расход в кислых растворах достигает 11 - 12 моль на 1 моль вещества. [2]
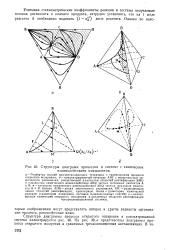 |
Структуры диаграмм процессов в системе с химическим. [3] |
Учитывая стехиометрические коэффициенты реакции и составы получаемых потоков дистиллята и нижнего продукта, нетрудно установить, что на 1 моль реагента А необходимо подавать ( l - хА3) моль реагента. [4]
Когда стехиометрические коэффициенты реакции перехода окисленной формы в восстановленную не равны единице, они входят в уравнение как показатели степеней соответствующих концентраций. При участии ионов водорода в реакции окисленная форма переходит в восстановленную с изменением состава иона окислителя или иона восстановителя. Электродный потенциал в этом случае зависит также и от концентрации ионов водорода. [5]
Поэтому нахождение стехиометрических коэффициентов реакций окисления-восстановления часто оказывается непростой задачей, которую решают с применением специально разработанных приемов. Рассмотрим метод полуреакций, обычно применяемый к реакциям в водных растворах. [6]
Связи между стехиометрическими коэффициентами реакции и ее частным и общим порядками в общем случае не существует. Порядок определяется только механизмом процесса, а экспериментальное определение частных порядков - первая и обязательная стадия изучения реакции. [7]
К, - стехиометрические коэффициенты реакций, / и г-времн и радиальная координата, отсчитываемая от центра скважины. [8]
 |
Зависимость равновесной. [9] |
Если исходить из стехиометрических коэффициентов реакции ( 1) и применять паро-газовую смесь с равными концентрациями водяного пара и окиси углерода, то, как следует из рис. V-2, степень превращения СО получается довольно низкой. Поэтому практически применяют паро-газовые смеси со значительным избытком водяного пара. [10]
Если исходить из стехиометрических коэффициентов реакции и применять парогазовую смесь с равными концентрациями водяного пара и оксида углерода, то степень превращения СО получается довольно низкой. Поэтому практически применяют парогазовую смесь со значительным избытком водяного пара. [11]
С целью нахождения стехиометрического коэффициента реакции в случае N-винилпирролидона был использован распространенный в аналитической химии графический метод. [12]
Молекулярность определяется суммой стехиометрических коэффициентов реакции. [13]
Здесь V; - стехиометрические коэффициенты реакции ( как обычно, для продуктов реакции они берутся со знаком плюс, для исходных веществ - со знаком минус): и. [14]
ПСу-произведение концентраций в степенях стехиометрических коэффициентов реакции; Л - газовая постоянная, равная 8 314 Дж / моль град. [15]
Страницы: 1 2 3 4