Диаграмма - энергетические уровни
Cтраница 2
Диаграмма энергетических уровней кремния, на которой показана энергия гибридизовашшх состояний оборванных связей, лежащая несколько выше дна зоны проводимости. Реконструкция приводит к расщеплению каждого такого уровня на два уровня, лежащих далеко от запрещенной зоны, причем на уровне с энергией es находятся два электрона, а другой уровень с энергией ер является незанятым. В общем случае следует ожидать, что эти уровни будут выталкиваться из запрещенной зоны. [16]
Диаграмма энергетических уровней атома водорода изображена на рис. 2.1. Состояния с 31, примыкающие к границе непрерывного спектра, соответствуют слабо связанному электрону, сильно удаленному от силового центра. [17]
 |
Параметры гетероатомов н образуемых ими связей, применяемые i методе МОХ. [18] |
Диаграмма энергетических уровней молекулы формальдегида в сравнении с этиленом приведена на рис. 8.11. Из диаграммы видно, что увеличение электроотрицательности одного из атомов в сопряженной системе приводит к проседанию уровней. [19]
Диаграмма энергетических уровней орбиталей октаэдрических молекул или ионов XY6, имеющих Зй-электроны, была уже приведена на фиг. Такого же типа молекулярные орбитали получаются и из а-компонент шести 2р - орбиталей. [20]
Постройте диаграммы энергетических уровней и покажите, как заселены d - орбитали иона-комплексообразователя в следующих случаях: d4, октаэдрическое поле, низкоспиновый комплекс; ds, тетраэдрическое поле, высокоспиновый комплекс; d7, октаэдрическое поле, высокоспиновый комплекс. [21]
Эта диаграмма энергетических уровней имеет несколько важных особенностей. Во-первых, заданный порядок уровней нужно независимо прилагать к нейтронам и протонам. На абсолютной шкале энергий протонные уровни располагаются все выше и выше нейтронных по мере роста Z. Это - знакомый уже эффект кулоновского отталкивания и в первом приближении он не вносит изменений в порядок уровней для каждого данного типа нуклонов. Однако имеется слабая тенденция к дополнительной стабилизации в ядрах с большим Z протонных уровней с максимальным орбитальным моментом ( 1 /, ig, Ih, li), обладающих здесь относительно меньшей энергией, поскольку при движении в наиболее удаленной от центра ядра области протоны в меньшей степени испытывают кулоновское отталкивание. [22]
Нарисуйте диаграмму энергетических уровней для цезиевого катода и с ее помощью рассчитайте наименьшую энергию WMHH ( вт-сек), которую необходимо подвести к рассматриваемому электрону, чтобы последний был эмиттирован. [23]
Постройте диаграмму энергетических уровней для поверхности GaAsv аналогичную диаграмме энергетических уровней для Si, которая изображена на рис. 10.9, и укажите энергию гибридизованных состояний оборванных связей до и после реконструкции. [24]
 |
Вандерваальсовы радиусы неметаллов ( А. [25] |
Нарисуйте диаграмму энергетических уровней для взаимодействия двух атомов, каждый из которых имеет s - орбиталь. [26]
Согласно диаграмме энергетических уровней, изображенной на рис. 9 - 2, бз-орбиталь более устойчива, чем 5с / - орбиталь, что не удивительно, поскольку аналогичное явление наблюдается в предыдущих периодах. Однако 4 / - орбитали обычно также устойчивее, чем 5 -орбитали, хотя различие между ними по энергии невелико и имеются исключения. Идеализированная схема заселения орбиталей у элементов шестого периода такова: сначала происходит заселение бз-орбитали у цезия, Cs, и бария, Ва, затем заселяются глубоко погруженные в общее атомное электронное облако 4 / - орбитали у 14 внутренних переходных элементов от лантана, La, до иттербия, Yb. Как показано на рис. 9 - 3, имеются незначительные отклонения от этой схемы. Наиболее важным из них является то, что после Ва новый электрон у La поступает на 5 -орбиталь, а не на 4 / - орбиталь. Поэтому лантан в сущности должен характеризоваться скорее как переходный, а не как внутренний переходный металл. Однако имеет больше смысла запомнить идеализированную схему заполнения, чем концентрировать внимание на отдельных исключениях из нее. [27]
На диаграмме энергетических уровней 16л - электро-нов помещены, начиная с нижнего уровня, по 2 электрона на каждом уровне. Первый незанятый уровень имеет энергию 0 24 J3 ( - 0 18 эв) по отношению к нулевому а. Одноэлектронную волновую функцию, соответствующую этой энергии, можно рассчитать, как описано в приложении. [28]
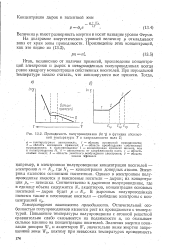 |
Проводимость полупроводников ( In - у в функции абсолютной температуры Т и напряженности поля Е. i. [29] |
На диаграмме энергетических уровней величину i откладывают вниз от края зоны проводимости. [30]
Страницы: 1 2 3 4 5