Атом - кислота
Cтраница 2
Прежде всего, Лоран подвергает резкой критике общепринятые тогда формулы для кислот, доказывая, что, предлагая их, химики исходили из априорного правила о нейтрализации одного атома кислоты одним атомом основания. [16]
Происхождение седьмой добавочной метильной группы было исследовано путем использования в качестве субстрата 5 - С14 - 6-аминолевулиновой кислоты; судя по предварительным результатам этих опытов, эта метильная группа ведет свое происхождение от б-углеродного атома б-аминолеву-линовой кислоты. [17]
Как отмечает А. И. Шатенштейн, отличительным признаком кислот и оснований, по электронной теории, является их взаимная нейтрализация, осуществляемая путем образования ковалентной связи между атомом основания, обладающим свободной парой электронов, и атомом кислоты, в дефицитную электронную оболочку которой включается эта пара электронов. [18]
Фосфорная кислота ( под которой обычно подразумевают ортокислоту, если при ней нет приставки мета - или пиро -) представляет собой трехосновную кислоту, образующую соли, в которых один, два или три водородных атома кислоты могуч1 быть замещены металлом. Соли, подобные NaHsPOi и Са ( Н РО4) 2, называют первичными фосфатами, а также одно-замещенными или одноосновными фосфатами. Соли, подобные N32HPO4 и СаНРО, называют вторичными, а также двузамещенными или двухосновными фосфатами. Наконец, соли, подобные NasKO и СазФСЬЬ, являются третичными ( трехзамещенными, трехосновными) фосфатами. [19]
Дело в том, что система 1826 г. привела к тому, что большинство сильных оснований должны были быть сведены к более простому составу: из одного атома радикала и одного атома кислорода; а их соли - к одному атому основания и одному атому кислоты. [20]
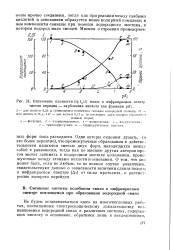 |
Оптические плотности ( ig 10 / 7 полос в инфракрасном спектр систем пиридин - карбоновая кислота как функция - рКг. [21] |
Одни авторы склонны думать, ( и это более вероятно), что промежуточные образования в действительности являются смесью двух форм, находящихся между собой в равновесии, тогда как по мнению других авторов протон может занимать в водородном мостике положения, промежуточные между атомами кислоты и основания. О том, что оно может быть, если не любым, то во всяком случае различным, свидетельствуют данные о зависимости величины сдвига полосы в инфракрасном спектре ( Av) от силы протолита, к рассмотрению которого перейдем. [22]
Дальтон полагает, что она обладает свойствами, которые отличают ее от всех других кислот. О кислоте, состоящей из 1 атома кислоты и 2 атомов воды, Дальтон говорит, что она обладает замечательными особенностями; в ней наблюдается полное взаимное насыщение двух компонентов. [23]
Хиггинсу, каждый из атомов кислоты помещается между атомами щелочи и находится в контакте с этими атомами, и наоборот. В таком соединении силы взаимного притяжения разнородных атомов кислоты и щелочи приблизительно соответствуют по величине силам взаимного отталкивания однородных атомов кислоты или щелочи. Из этого принципа следует, что не может иметь места дополнительное присоединение атомов кислоты или щелочи ( с, d, e), так как они не могут удерживаться компенсирующими силами притяжения других атомов. В этом случае образуется соединение в виде агрегата - abababab, и это соединение не способно к присоединению посторонних атомов. [24]
Атомные веса бериллия и урана были установлены совершенно неверно. Для окиси бериллия была не только дана неправильная формула ВеОз ( так как Берцелиус считал, что в минералах, содержащих бериллий, окись бериллия соединяется с тремя атомами кислоты), но и анализ окиси был проведен неверно. [25]
При перегонке жидкость эта дает кислый дестиллят, на котором плавают масловидные капли. Дестиллят, насыщенный углекислым натром и выпаренный досуха, оставляет чистые соли летучих кислот С НпО - - Для разделения кислот, раствор натронных солей был осаждаем, мало-помалу, азотнокислой окисью серебра, каждый осадок серебряной соли собран отдельно и по высушивании подвергнут сожиганию для определения веса атома кислот. Две из этих солей дали числа соответствующие - одна уксусной, другая - валериановой кислоте; остальные результаты были промежуточные, и, следовательно, эти последние соли представляли смеси. Тем не менее, однакон, опыт этот дает полное право заключить, что при действии расплавленного едкого кали на масло Pulegii deserli-colae образуются летучие кислоты дигенильного ряда - уксусная и валериановая и, вероятно, также промежуточные члены. [26]
Электронная теория обобщенных кислот и оснований устанавливает связь между кислотными и основными свойствами веществ и их строением. Основания являются донорами пары электронов, а кислоты акцепторами пары электронов. Нейтрализация состоит в образовании координационной ковалентной связи между атомом основания и атомом кислоты. [27]
При выводе своих формул Волластон в известной мере руководствовался правилом Берцелиуса о том, что в средних солях кислород кислоты является целым кратным кислорода основания. Волластон придерживался также того положения, что средняя соль образована одним атомом кислоты и одним атомом основания. [28]
Хиггинсу, каждый из атомов кислоты помещается между атомами щелочи и находится в контакте с этими атомами, и наоборот. В таком соединении силы взаимного притяжения разнородных атомов кислоты и щелочи приблизительно соответствуют по величине силам взаимного отталкивания однородных атомов кислоты или щелочи. Из этого принципа следует, что не может иметь места дополнительное присоединение атомов кислоты или щелочи ( с, d, e), так как они не могут удерживаться компенсирующими силами притяжения других атомов. В этом случае образуется соединение в виде агрегата - abababab, и это соединение не способно к присоединению посторонних атомов. [29]
Последний термин не требует особых пояснений. К окислителю полностью переходит один или несколько электронов восстановителя, а один из атомов кислоты или кислотоподобного вещества разделяет с атомом основания его свободную электронную пару. При реакции кислоты по схеме Бренстеда одновременно разрывается химическая связь между атомом водорода и кислотным остатком, и к электронной паре основания присоединяется протон. Во время реакции с кислотоподобным веществом, например с фтористым бором, электроны основания восполняют электронный дефицит у атома бора и возникает ковалентная связь. [30]
Страницы: 1 2 3