Атом - медь
Cтраница 1
Атомы меди находятся либо в квадратной пирамиде CuOs, либо в центре плоских квадратов СиСМ, образующих чередующиеся слои. [1]
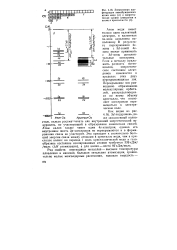 |
Электронная конфигурация невозбужденного атома меди ( а и энергетические уровни электронов в атоме и кристалле Си ( б. [2] |
Атом меди имеет только один валентный электрон, и валентная 45-зона заполнена наполовину. Если к металлу приложить разность потенциалов, энергетическое состояние электронов изменяется в пределах этих двух перекрывающихся зон. Перекрывание зон равноценно образованию молекулярных орбита-лей, распределяющихся по всему объему кристалла, что позволяет электронам перемещаться в электрическом поле. [3]
Атомы меди, серебра и золота могут проявлять более высокую степень окисления, чем атомы элементов главной подгруппы. Валентными электронами могут являться не только ns - электроны, но и ( п - 1 -электроны, так как энергии ( п -) d - и ns - электронов близки. [4]
Атомы медя, серебра и золота имеют по одному легко отделяющемуся валентному s - электрону, образующему электронный газ, который связывает однократно заряженные положительные ионы, обладающие внешними 110-подоболочками. Низкая концентрация электронного газа не обеспечивает сближения этих ионов до перекрытия и взаимодействия их внешних d - электронных облаков. Упаковка этих псевдосферических ионов ненаправленными еила. Диаметры атомов и параметры решеток возрастают от меди к серебру и слепка уменьшаются от серебра к золоту вследствие лантанидного сжатия электронных оболочек, вызываемого увеличением заряда ядра при застройке внутренней 4 / - лодоболочки, которая ведет к усилению притяжения внешних электронов. [5]
Атомы меди в молекулах хлорной меди или медного купороса могут замещаться не только железом; легко замещают их атомы цинка и некоторых других металлов. [6]
Атом меди в ( CO) 3MnCBH4Cu заменяется на HgCl и ферроценильный радикал. [7]
Атомы меди, серебра и золота имеют на внешнем слое 1 электрон и в этом отношении проявляют структурное сходство с атомами щелочных металлов. Однако у атомов щелочных металлов в слое, соседне м с наружным, находится 8 электронов, а у атомов меди, серебра и золота этот слой содержит 18 электронов. Этим объясняется резкое отличие свойств рассматриваемых здесь элементов от свойств щелочных металлов. Для наглядности сопоставим калий и медь. [8]
Атомы меди, серебра и золота имеют на внешнем слое 1 электрон, и в этом отношении проявляют структурное сходство с атомами щелочных металлов. Однако у атомов щелочных металлов в слое, соседнем с наружным, находится 8 электронов, а у атомов меди, серебра и золота этот слой содержит 18 электронов. Этим объясняется резкое отличие свойств рассматриваемых здесь элементов от свойств щелочных металлов. Для наглядности сопоставим калий и медь. [9]
Атомы меди, серебра и золота имеют на внешнем слое 1 электрон и в этом отношении проявляют структурное сходство с атомами щелочных металлов. Однако у атомов щелочных металлов в слое, соседнем с наружным, находится 8 электронов, а у атомов меди, серебра и золота этот слой содержит 18 электронов. Этим объясняется резкое отличие свойств рассматриваемых здесь элементов от свойств щелочных металлов. [10]
Атомы меди, серебра и золота имеют на внешнем слое 1 элек - TDOH и в этом ОТНПШРНИИ проявляют структурное сходство с атомами щелочных металлов. Однако у атомов щелочных металлов в слое, соседнем с наружным, находится 8 электронов ( у лития-2), а у атомов меди, серебра и золота этот слой содержит 18 электронов. Этим объясняется резкое отличие свойств рассматриваемых здесь элементов от свойств щелочных металлов. [11]
Атомы меди, серебра и золота имеют на внешнем слое 1 электрон и в этом отношении проявляют структурное сходство с атомами щелочных металлов. Однако у атомов щелочных металлов в слое, соседнем с наружным, находится 8 электронов ( у лития-2), а у атомов меди, серебра и золота этот слой содержит 18 электронов. Этим объясняется резкое отличие свойств рассматриваемых здесь элементов от свойств щелочных металлов. [12]
Атом меди ( № 29) имеет три заполненные оболочки ( п1, 2, 3, с числом электронов 2, 8, 18), и, кроме того, в первом слое четвертой оболочки имеется один элек трон. [13]
Атом меди отдает два электрона двухатомной молекуле хлора. Хлор восстанавливается и выступает в роли окислителя. Медь окисляется и является восстановителем. [14]
Атомы меди располагаются в вершинах и центрах граней куба, а атомы хлора находятся в центрах четырех из восьми октантов. Каждый атом хлора непосредственно связан с четырьмя атомами меди, и, наоборот, каждый атом меди - с четырьмя атомами хлора. В результате в твердом хлориде меди элементы проявляют валентность, равную четырем. [15]
Страницы: 1 2 3 4