Атом - медь
Cтраница 2
Атом меди ( 1) образует три связи также в некоторых сульфидах ( о характере этих связен см. последний раздел данной главы), атом серебра ( 1) - в некоторых серосодержащих соединениях; здесь также не всегда удается дать простую интерпретацию картины связей. [16]
Атомы меди немного смещены в сторону тетраэдрических пустот, и в дополнение к трем атомам серы в окружение меди входят два соседних атома меди на расстоянии 2 64 А и еще два на расстоянии 2 97 А. В гексагональном халькозине - П атомы меди статистически распределены по трем типам полостей в гексагональной плотнейшей упаковке атомов серы. Кроме того, расстояние между 3 - и 4-координировапны-ми атомами меди составляет всего 2 59 А. [17]
Атом меди в медьорганических соединениях имеет тенденцию координироваться с донорными частицами. [18]
Атом меди в медьорганических соединениях образует координационные связи с донорными частицами. Например, алкилмедь взаимодействует с ли-тийорганическими соединениями с образованием литийдиалкилкупратов. [19]
Атомы меди располагаются в вершинах и центрах граней куба, а атомы хлора находятся в центрах четырех из восьми октантов. Каждый атом хлора непосредственно связан с четырьмя атомами меди, и, наоборот, каждый атом меди - с четырьмя атомами хлора. В результате в твердом хлориде меди элементы проявляют валентность, равную четырем. [20]
Атомы меди совершают колебания в трех направлениях относительно положения равновесия в узлах решетки. [21]
Атомы меди, серебра и золота, как и атомы щелочных металлов, имеют во внешнем электронном слое один электрон. Структура же предпоследних электронных слоев у металлов той и другой подгрупп различна. Если у атомов щелочных металлов предпоследний слой состоит из 8 электронов ( у лития - 2 электрона), то у элементов подгруппы меди он состоит из 18 электронов. Этим объясняется резкое отличие в свойствах элементов обеих подгрупп. [22]
 |
Структурный тип СаТЮ3.| Структурный тип К3 [ Со ( NOS ]. [23] |
Атомы меди в структуре СиА12 и калия в структуре KHF2 имеют координационное число 8 и помещаются в многограннике, называемом томсоновским кубом. [24]
Атом меди отдает 2 электрона двухатомной молекуле хлора. Хлор восстанавливается и выступает в роли окислителя. Медь окисляется и является восстановителем. [25]
 |
Схема строения атома алюминия. [26] |
Атом меди содержит 29 электронов и такое же количество протонов. Электроны атомов меди расположены вокруг ядра на четырех оболочках. На первой находятся два электрона, на второй - восемь, на третьей - восемнадцать, на четвертой, наиболее удаленной от ядра, - один электрон. Число электронов, расположенных на наиболее удаленной от ядра оболочке, совпадает с номером группы данного элемента в периодической системе Д. И. Менделеева, а общий отрицательный заряд электронов атома равен положительному заряду протонов, содержащихся в ядре. Равные по величине положительные и отрицательные заряды по отношению к внешней среде электрически уравновешиваются - взаимно нейтрализуются. В результате этого атомы вещества в обычном состоянии электрически нейтральны. [27]
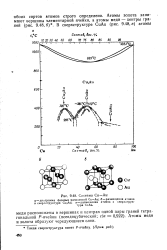 |
Система Си-Аи. [28] |
Атомы меди и золота образуют чередующиеся слои. [29]
Атом меди отдает два электрона двухатомной молекуле хлора. Хлор восстанавливается и выступает в роли окислителя. [30]
Страницы: 1 2 3 4