Атом - переходный металл
Cтраница 1
Атомы переходных металлов имеют девять валентных орбиталей ( п -) d nsr и п / 73 и при образовании связей стремятся их использовать. Связи М - С являются сг-связями, они образуются в результате перекрывания вакантных орбиталей атома металла атома углерода с неподеленной парой электронов. Так, соединения [ Ni ( CO) 4j, [ Fe ( CO) 5 ], [ Сг ( СО) 6 ] образуют в пространстве соответственно тетраэдр, триго-нальную бипирамиду, октаэдр, причем образуется четыре, пять и шесть 0-связей. [1]
Атомы переходных металлов могут служить центрами для реакций окислительного присоединения и восстановительного элиминирования. По аналогии с ис-присоединением водорода к координационно ненасыщенным комплексам переходных металлов, протекающим, по всей вероятности, в виде согласованною процесса, обычно полагают, что одностадийное г ис-присоединение является общим механизмом всех этих процессов. [2]
Атомы переходных металлов характеризуются существованием внутренних незаполненных электронных уровней. [3]
Атомы переходных металлов этой группы имеют два или один электрон на внешней оболочке и незастроенную предшествующую оболочку. Связь в их кристаллах металлическая, решетка пространственно центрированная кубическая. [4]
Атом переходного металла участвует в образовании связей девятью орбиталями: пять md, одна ( m l) s и три ( т) р, где т 3 - 5 обозначает период. Три ейэрбитали аксиально-симметричного фрагмента МЬЛ не смешиваются с орбиталями лигандов и образуют низко лежащий, слабо расщепленный уровень, который близко соответствует 12 -урова. [5]
Все атомы переходных металлов имеют один или два электрона на самой внешней оболочке и поэтому ведут себя прежде всего, как металлы. Большинство из них имеет два электрона в крайней оболочке, а большая часть остальных с химической точки зрения может рассматриваться как имеющая тоже два электрона. Сходство их, когда они выступают в роли катионов, уже было разобрано. [6]
Некоторые атомы переходных металлов являются сильными тг-кислотами ( тг-акцепторами) и образует прочную связь с органическими тт-основаниями. В случае f - переходных металлов ряда актиноидов считается возможным участие / - орбиталей в образовании связей с лигандом. [7]
Электроположительность атома переходного металла увеличивается по мере уменьшения его валентности; поэтому только низковалентные соединения переходных металлов могут действовать в координационном катализе анионного типа. Слабоэлектроположительные металлы ( например, Pt, Pd и др.) даже в низковалентном состоянии неактивны. [8]
M - атом переходного металла - конфигурации. [9]
В оксинитридах атом переходного металла должен образовать пять ковалентных и три донорно-акцепторные связи с мостиковыми атомами. Поэтому X может быть элементом V-VII групп. В оксинитридах все зоны уровней, возникшие в результате образования я-связей в кумулированных цепях, заполнены электронами, и в слое электрическая проводимость не может иметь места. [10]
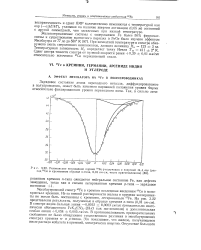 |
Резонансное поглощение ядрами 67Fe у-излучения с энергией 14 4 кэв ( распад 57Со в кремниевом образце п-типа, 0 01 ом-см, чисто приготовленном. [11] |
Зарядовое состояние атома переходного металла, диффундировавшего в полупроводник, может быть изменено вариацией положения уровня Ферми относительно фиксированного уровня переходного иона. [12]
Если вместо атома переходного металла X использовать атом элемента третьего периода ( скажем, фосфора), то все связи с мостиковыми атомами не могут быть полностью двойными. В этом случае цепи таких связей уже не будут прямолинейными, а, следовательно, и вся система не может быть плоской. Весьма вероятно, что такое неплоское строение имеет полученное недавно вещество состава PON [129], где атом Р должен находиться в окружении, близком к тетраэд-рическому. [13]
Соединения, включающие атом переходного металла и два цикло-пентадиенильных кольца, связанных с металлом сэндвичеобразно. [14]
В этих соединениях атом переходного металла ( у которого в основном состояния заняты ( п - 1) d - и / zs - орбитали, п 3, 4, 5) окружен лигандами ( чаще всего это атомы галогена или кислорода), для которых валентными являются s - и р-орбитали. Включение в базис виртуальных ( вакантных в атоме) весьма диффузных пр-орбиталей металла приводит к заниженным зарядам на металле ( иногда даже отрицательным) в силу упомянутых особенностей малликеновского анализа заселенностей. [15]
Страницы: 1 2 3 4