Атом - фтор
Cтраница 2
Атом фтора имеет в наружной электронной оболочке 7 валентных электронов, как и атомы хлора, брома и иода. [16]
Атомы фтора не обмениваются при вращении. Это можно увидеть, применив критерий замещения для диастереотопных групп; замещение атома F на хлор в любом из трех конформеров ( XlVa - Х1Ув) всегда приводит к тирео-изомеру ВгСШС - CFClBr, тогда как аналогичное замещение атома F всегда дает вритро-изомер. [17]
Атом фтора в некоторых азотсодержащих гетероциклах настолько подвижен, что конечное фторсодержащее соединение выделить не удается из-за побочных реакций. [18]
Атомы фтора сильно снижают также реакционную способность других атомов галоида, находящихся у одного и того же атома углерода. [19]
Атомы фтора в соединениях типа ( II) очень подвижны и легко омыляются. Это обстоятельство используют для обмена гндрооксилыгой группы на фтор. [20]
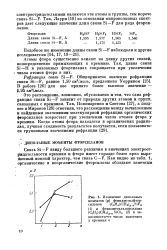 |
Изменение дипольных моментов ( ц фенилметилфтор-силанов ( C6H5 ( CH3 3 nSiFn. [21] |
Атомы фтора существенно влияют на длину других связей, непосредственно примыкающих к кремнию. Так, длина связи Si - Н в указанных фторсиланах сокращается при увеличении числа атомов фтора в них. [22]
Атомы фтора, связанные с кремнием или находящиеся в органических радикалах, оказывают большое влияние на колебательные частоты соседних связей, как правило, в сторону их повышения. [23]
Атомы фтора в большей степени повышают электрофильность атома кремния, чем атомы хлора. Это облегчает нуклеофильную атаку со стороны FeCl, ведущую к отщеплению силильной группы, если катион ( С1) присоединился к атому углерода, связанному с силильной группой. [24]
Атомы фтора ( и трифторметильные группы в целом) проявляют отрицательный индукционный эффект, оттягивают на себя электронную плотность и тем самым делают атом водорода заряженным положительно, который затем отщепляется в виде протона. [25]
Атомы фтора экранируют связи С-С в макромолекулах, что значительно повышает стойкость полимера к деструкции. [26]
Атом фтора сильно отличается от других галоидов и по своему влиянию на 1с мо2 эквивалентен атому водорода. [27]
Атомы фтора могут содержаться в диольном или диизо-циаяатном звеньях или в обоих звеньях одновременно. [28]
Атомы фтора оказывают сильное влияние на энергию и реакционную способность не только С-С - связи, но и всех других химических связей в молекулах. Характерной особенностью частично фторированных углеводородов является образование водородных связей между атомами водорода и фтора. Энергия этих водородных связей довольно высока из-за сильной поляризации связи С - Н и большой электроотрицательности атома фтора. [29]
Атомы фтора, обладающие большей ЭО, чем углерод, равномерно ттягивают его валентные электроны и образуют полярные связи С - F. Если один из атомов F заменить на атом водорода, то естественно, что в молекуле CHF3 три атома фтора будут испытывать очень слабую конкуренцию со стороны Н ( ЭО которого значительно меньше, чем F) в оттягивании электронов от углерода, в результате чего полярность связей С-F во фтороформе будет больше, чем в четырехфтористом углероде. Очевидно, что в CH3F этот эффект будет максимальным. [30]
Страницы: 1 2 3 4