Атом - элемент - подгруппа
Cтраница 2
Атомы элементов подгруппы II IB характеризуются электронной конфигурацией ( п -) dlnsz. [16]
 |
Свойства элементов подгруппы бериллия. [17] |
Атомы элементов подгруппы бериллия на внешнем уровне имеют по два электрона. Все металлы подгруппы - сильные восстановители, однако несколько более слабые, чем щелочные металлы. [18]
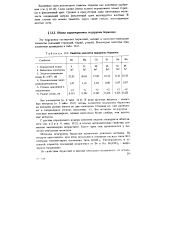 |
Свойства эделентов подгруппы бериллия. [19] |
Атомы элементов подгруппы бериллия на внешнем уровне имеют по два электрона. Все металлы подгруппы - сильные восстановители, однако несколько более слабые, чем щелочные металлы. [20]
Радиусы атомов элементов подгруппы незначительно отличаются от величин у предшествующих элементов периодической системы. Радиусы же ионов меньше, чем у щелочных металлов тех же периодов и нарастают по подгруппе сверху вниз. Си к Аи и нарастает с увеличением заряда катиона. Заряды ядер значительно выше, чем у щелочных металлов тех же периодов. Отсюда вытекают особенности свойств соединений этих элементов. Основные свойства гидроксидов у них выражены слабее, возрастают от Си к Ag и уменьшаются по мере увеличения заряда катиона. [21]
В атомах элементов подгруппы ванадия продолжается достройка предпоследнего электронного слоя: он пополняется еще одним электроном. В качестве валентных у этих элементов могут выступать, помимо двух электронов внешнего слоя, три электрона достраивающегося слоя. [22]
Аналогичным образом атомы элементов подгруппы VB образуют двуслойные пакеты, в которых каждый атом связан с тремя ближайшими соседями ковалентными связями. При объединении этих пакетов получается трехмерная структура, например ромбоэдрическая типа А7, которая характерна для мышьяка, сурьмы и висмута ( фиг. Цепи в структуре типа А8 и пакеты в структуре типа А 7 связаны друг с другом относительно слабыми связями Ван-дер - Ваальса, на которые накладывается в незначительной степени металлическая связь. В результате получаются структуры, обладающие значительной анизотропией физических свойств. XIII и XVI х) и обусловливает значительно большую хрупкость элементов подгрупп VB и VIВ по сравнению с элементами, обладающими типичными металлическими структурами. [23]
Чем отличаются атомы элементов подгруппы скандия от атомов элементов главной подгруппы III группы по строению электронных оболочек. Как это сказывается на их свойствах. [24]
Аналогичным образом атомы элементов подгруппы VB образуют двуслойные пакеты, в которых каждый атом связан с тремя ближайшими соседями ковалентными связями. При объединении этих пакетов получается трехмерная структура, например ромбоэдрическая типа А -, которая характерна для мышьяка, сурьмы и висмута ( фиг. Цепи в структуре типа А & и пакеты в структуре типа А 7 связаны друг с другом относительно слабыми связями Ван-дер - Ваальса, на которые накладывается в незначительной степени металлическая связь. В результате получаются структуры, обладающие значительной анизотропией физических свойств. XIII и XVI х) и обусловливает значительно большую хрупкость элементов подгрупп VB и VIB по сравнению с элементами, обладающими типичными металлическими структурами. [25]
В химических реакциях атомы элементов подгруппы легко отдают оба электрона внешнего энергетического уровня и образуют. [26]
Вследствие такой структуры атомы элементов подгруппы ванадия не обнаруживают склонности к дополнению внешнего квантового слоя до восьми электронов. [27]
В основном состоянии атомы элементов подгруппы германия имеют строение внешних электронных оболочек 4s24p2 ( Ge), 5s25p2 ( Sn), 6s26p2 ( Pb) и двухвалентны. [28]
В основном состоянии атомы элементов подгруппы галлия имеют строение внешних электронных оболочек 4s24p ( Ga), 5s25p ( In), 6s26p ( Tl) и одновалентны. Возбуждение трехвалентных состояний требует затраты 108 ( Ga), 100 ( In) или 129 ( TI) ккал / г-атом. Сродство атома таллия к электрону оценивается в 12 ккал / г-атом. [29]
В основном состоянии атомы элементов подгруппы германия имеют строение внешних электронных оболочек 4s24 / J2 ( Ge), 5s25p2 ( Sn), 6s26p2 ( Pb) и двухвалентны. [30]
Страницы: 1 2 3 4