Атом - элемент - подгруппа - медь
Cтраница 1
Атомы элементов подгруппы меди имеют еще одну особенность. Предпоследний 18 - й электронный слой у них еще не вполне устойчив и способен к частичной потере электронов. [1]
Радиусы атомов элементов подгруппы меди значительно меньше радиусов атомов щелочных металлов, что обусловлено наличием восемнадцати электронов на их предпоследнем слое. Поэтому для меди и ее аналогов характерны значительно большие значения ионизационного потенциала и сродства к электрону, чем для щелочных металлов. Это обстоятельство является важнейшей причиной различия в свойствах элементов подгруппы меди и щелочных металлов. [2]
Электронная структура атомов элементов подгруппы меди может быть выражена формулой... [3]
Это связано с особенностями структуры атомов элементов подгруппы меди и с относительными размерами их. [4]
Чем отличаются электронные структуры атомов щелочных металлов от электронных структур атомов элементов подгруппы меди. Как отражаются электронные структуры этих подгрупп на Свойствах их гидроокисей и на способности этих элементов образовывать комплексные соединения. [5]
Чем отличаются электронные структуры атомов щелочных металлов от электронных структур атомов элементов подгруппы меди. Как влияют электронные структуры этих атомов элементов подгрупп на свойства их гидроксидов и на способность этих элементов образовывать комплексные соединения. [6]
У атомов цинка, кадмия и ртути, как и у атомов элементов подгруппы меди, d - подуровень второго снаружи электронного слоя целиком заполнен. [7]
У атомов цинка, кадмия и ртути, как и у атомов элементов подгруппы меди, rf - подуровень второго снаружи электронного слоя целиком заполнен. Однако у элементов подгруппы цинка этот подуровень уже вполне стабилен и удаление из него электронов требует очень большой затраты энергии. Ртуть, кроме того, образует соединения, в которых ее степень окис-ленности равна - f - 1; но, как будет показано ниже ( см. § 216), и в этих соединениях ртуть следует считать двухвалентной. [8]
У атомов цинка, кадмия и ртути, как и у атомов элементов подгруппы меди, d - подуровень второго снаружи электронного слоя целиком заполнен. [9]
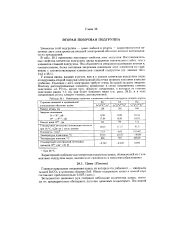 |
Некоторые свойства элементов побочной подгруппы второй группы. [10] |
У атомов цинка, кадмия и ртути, как и у атомов элементов подгруппы меди, d - подуровень второй снаружи электронной оболочки целиком заполнен и вполне стабилен. Удаление с него электронов требует очень большой затраты энергии. Ртуть, кроме того, образует соединения, в которых ее степень окисления равна 1; но, как будет показано ниже ( см. разд. [11]
Чем отличаются электронные структуры атомов ш лочных металлов от электронных структур атомов элементов подгруппы меди. Как отражаются электронные структуры этих подгрупп на свойствах их гидроокисей и на способности этих элементов образовывать комплексные соединения. [12]
У атомов цинка, кадмия и ртути, как и у атомов элементов подгруппы меди, d - подуровень второго снаружи электронного слоя целиком заполнен. [13]
Медь Си, серебро Ag и золото Аи каждый в своем периоде являются предпоследними - элементами. Таким образом, в атомах элементов подгруппы меди в ( п - 1) rf - состоянии должны находиться по девять электронов. Однако вследствие устойчивости ( / - конфигурации энергетически оказывается более выгодным переход одного из ns - электронов в ( п - 1) rf - состояние. Поэтому Си, Ag и Аи в s - состоянии внешнего слоя имеют по одному, а в предпоследнем слое по 18 ( s2 6 10) электронов. [14]
Медь Си, серебро Ag и золото Аи каждый в своем периоде являются предпоследними of - элементами. Таким образом, в атомах элементов подгруппы меди в ( - 1) - состоянии должны находиться по девять электронов. Однако вследствие устойчивости с ( 10-конфигу-рации энергетически оказывается более выгодным переход одного из s - электронов в ( п - 1) с. Поэтому Си, Ag и Аи в s - co - стоянии внешнего слоя имеют по одному, а в предпоследнем слое по 18 ( s2padw) электронов. [15]
Страницы: 1 2