Атом - элемент - главная подгруппа - группа
Cтраница 2
В табл. 63 приведены электронные структуры атомов элементов главной подгруппы VI группы. У этих атомов на последнем электронном слое 6 электронов а на предпоследнем - у кислорода 2, у серы 8, у селена, теллура и полония - по 18 электронов. В соединениях сера, селен, теллур и полоний могут быть двух -, четырех - и шестивалентными. [16]
Чем отличаются атомы элементов побочной подгруппы от атомов элементов главной подгруппы II группы по строению электронных оболочек. Почему потенциалы их ионизации больше, чем у атомов элементов главной подгруппы II группы, и как это сказывается на свойствах. [17]
Чем отличаются атомы элементов подгруппы скандия от атомов элементов главной подгруппы III группы по строению электронных оболочек. Как это сказывается на их свойствах. [18]
Чем отличается электронное строение атомов элементов побочной подгруппы IV группы от электронного строения атомов элементов главной подгруппы IV группы. Как это сказывается на их свой -, ствах. [19]
Атомы элементов главной подгруппы I группы имеют на валентной оболочке один электрон, а атомы элементов главной подгруппы II группы - два электрона. [20]
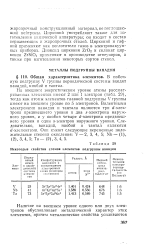 |
Некоторые свойства атомов элементов подгруппы ванадия. [21] |
На внешнем энергетическом уровне атомы рассматриваемых элементов имеют 2 или 1 электрон ( табл. 29), тогда как атомы элементов главной подгруппы V группы имеют на внешнем уровне по 5 электронов. Валентными электронами ванадия и тантала являются три d - элек-трона предвнешнего уровня и два s - электрона наружного уровня, а у ниобия четыре d - электрона предвнешнего уровня и один s - электрон наружного уровня. Следовательно, ванадий, ниобий и тантал являются d - элементами. [22]
 |
Некоторые свойства атомов элементов подгруппы ванадия. [23] |
На внешнем энергетическом уровне атомы рассматриваемых элементов имеют 2 или 1 электрон ( табл. 34), тогда как атомы элементов главной подгруппы V группы имеют на внешнем уровне по 5 электронов. Валентными электронами ванадия и тантала являются три rf - элек-трона предвнешнего уровня и два s - электрона наружного уровня, а у ниобия четыре d - электрона предвнешнего уровня и один s - электрон наружного уровня. [24]
Естественно предположить, что атомы этих элементов должны быть сходными и по строению. Атомы элементов главных подгрупп I-III групп периодической системы на внешнем энергетическом уровне имеют мало электронов ( 1 - 3) и, стремясь принять более устойчивое состояние ( структуру атомов инертных газов), сравнительно легко отдают эти электроны, превращаясь в положительно заряженные ионы. Эта особенность обусловливает своеобразное строение кристаллической решетки металлов, которая состоит из положительных ионов и атомов, находящихся в узлах решетки. Между узлами находятся электроны, не принадлежащие каким-либо определенным атомам. Малые размеры электронов позволяют им более или менее свободно перемещаться по всему кристаллу металла, переходя от одного атома или иона к другому атому или иону. При достаточном сближении электронов с ионами образуются нейтральные атомы, которые снова распадаются на ионы и электроны. [25]
Естественно предположить, что атомы этих элементов должны быть сходными и по строению. Атомы элементов главных подгрупп I-III групп периодической системы на внешнем энергетическом уровне имеют мало электронов ( 1 - 3) и, стремясь принять более устойчивое состояние ( структуру атомов инертных газов), сравнительно легко, отдают эти электроны, превращаясь в положительно заряженные ионы. Между узлами находятся электроны, не принадлежащие каким-либо определенным атомам. Малые размеры электронов позволяют им более или менее свободно перемещаться по всему кристаллу металла, переходя от одного атома или иона к другому атому или иону. При достаточном сближении электронов с ионами образуются нейтральные атомы, которые снова распадаются на ионы и электроны. [26]
Они образуются взаимодействием трех непарных р-электронов атома В и s - электронов трех атомов А. Три непарных электрона характерны для атомов элементов главной подгруппы V группы ( V А) азота и его аналогов. [27]
Как следует из спектральных термов, максимальная положительная трехвалент-ностъ рассматриваемых элементов объясняется, таким образом, тем, что эти и только эти три электрона могут отщепляться относительно легко. Общая работа, затрачиваемая на отрыв от атома элемента главной подгруппы III группы трех электронов, меньше ( см. табл. 63) работы, которую нужно затратить для отрыва одного следующего электрона. [28]
Чем отличаются атомы элементов побочной подгруппы от атомов элементов главной подгруппы II группы по строению электронных оболочек. Почему потенциалы их ионизации больше, чем у атомов элементов главной подгруппы II группы, и как это сказывается на свойствах. [29]
Замечательнейшая способность твердого вещества сохранять форму обусловлена тем, что его структура существует в довольно широком диапазоне изменений температуры и других условий, пока не разрываются связи между структурными единицами. Если это межатомные связи, то структура твердого вещества может обладать высокой устойчивостью. Именно благодаря исключительной прочности и жесткой направленности связей С - С, С - N, В - N, Р - N, Si - О, Si - О - Al, Fe - Fe, Ni - Сг, образованных sp - оболочками атомов элементов главных подгрупп III-VI групп и d - оболочками атомов переходных элементов, мы имеем целый арсенал превосходных материалов. Связь С - - С среди других межатомных связей выделяется так же ярко, как алмаз среди других твердых веществ. Благодаря ее прочности мы можем получать особо легкие жесткие материалы, обладающие в высшей степени ажурной структурой, химически стойкие и жаропрочные, каталитически активные и, наконец, биологически совместимые. На основе углерода природой созданы различные биоматериалы - прочнейшие живые ткани, например, кожа, шерсть, паутина; активнейшие реагенты - ферменты, гормоны; целые органы и сами организмы. [30]
Страницы: 1 2