Атом - неметаллический элемент
Cтраница 1
Атомы неметаллических элементов имеют большое число электронов ( 4 - 8) на внешнем энергетическом уровне. Лишь у водорода и гелия ( 1-ый период) на внешнем энергетическом уровне находится соответственно 1 и 2 электрона, у бора ( 2-ой период) - 3 электрона. Поэтому для элементов-неметаллов характерны большие значения энергий ионизации. [1]
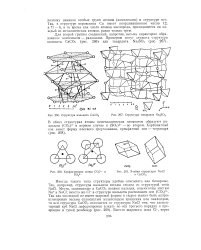 |
Структура кальцита СаСО3.| Структура тенардита Na2SO4.| Конфигурация ионов СО32 - и.| Ячейки структуры NaCl и СаСО3. [2] |
В обеих структурах атомы неметаллических элементов образуют радикалы ( СО3) 2 - в первом случае и ( SO4) 2 - - во втором. [3]
По Косселю, атомы неметаллических элементов, стремясь к октетной конфигурации, принимая недостающее до 8 число электронов, превращаются в отрицательный ион. [4]
Большинство молекул состоит из атомов неметаллических элементов. Эти атомы удерживаются вместе в результате притяжения ядра одного атома к электронам другого. Однако разница в силе притяжения электронов к атомам слишком мала для того, чтобы электроны полностью переместились от одного атома к другому. В результате, как это часто случается при взаимодействии металлических и неметаллических элементов, ионы не образуются. [5]
Ковалентная связь образуется преимущественно между атомами неметаллических элементов. [6]
Образование большого положительного заряда на атоме неметаллического элемента с высокой электроотрицательностью малоправдоподобно. [7]
Можно ожидать, что полимер, состоящий из атомов неметаллических элементов, будет напоминать полиэтилен ( СН2) и другие характерные полимеры. В некоторых отношениях это так и есть, но он обладает и некоторыми уникальными свойствами. Например, он имеет вид металла и проводит электрический ток так же хорошо, как металлическая ртуть. [8]
В атомах металлов внешние электроны удерживаются значительно слабее, чем в атомах неметаллических элементов. Металлы, как правило, имеют низкие потенциалы ионизации и выступают в качестве восстановителей. [9]
 |
Распространенность химических элементов в земной оболочке. [10] |
Молекулы воды HjO, аммиака МН, диоксида углерода COj построены из атомов различных неметаллических элементов ( см. 1.6), соединенных между собой ковалентными связями. Так, молекула воды HjO составлена из двух атомов водорода Н и одного атома кислорода О, причем атом кислорода образует отдельные ковалентные связи с каждым атомом водорода. [11]
В атомах металлов внешние электроны удерживаются значи -: / тельно слабее, чем в атомах неметаллических элементов. Металлы, - как правило, дмеют низкие потенциалы ионизации и выступают jB Ka4ecTBe восстановителей. [12]
Электронные структуры других молекул, имеющих ковалентные связи, можно легко записать, если учесть, что атомы неметаллических элементов должны иметь при этом заполненные октеты электронов. [13]
В общем можно представить себе гидридные ионы содержащими в качестве акцепторов электронов такие атомы, как бор, а также более сильные акцепторы электронов, как протоны или окисленные атомы неметаллических элементов. Поэтому идея гидрид-ного потенциала при оценке силы протонных кислот должна быть на первом плане, и когда-нибудь будет создана р-гидрид-ная шкала для ее измерения. [14]
При передаче электронов атомы металлического и неметаллического элементов стремятся сформировать вокруг своих ядер устойчивую конфигурацию электронной оболочки. Атом неметаллического элемента создает вокруг своего остова внешнюю оболочку последующего благородного газа ( электронный октет), тогда как атом металлического элемента после отдачи внешних электронов получает устойчивую октетную конфигурацию предыдущего благородного газа. [15]
Страницы: 1 2