Атом - неметаллический элемент
Cтраница 2
Установлено, что скорость диффузии в сплаве тем больше, чем / меньше атомный диаметр растворенного элемента. Например, атомы неметаллических элементов С, N, О, Н, диаметр которых меньше атомного диаметра железа, диффундируют в железо быстрее, чем атомы металлов. Поэтому температура, при которой про -; текает диффузия атомов неметаллических элементов, значительно) ниже температуры диффузии атомов металла; энергия активации при этом в несколько раз меньше. Скорость диффузии элемента находится в обратной зависимости от растворимости его в основном металле; она тем больше, чем дальше элементы расположены в периодической системе элементов Менделеева. [16]
Для второй группы соединений, напротив, весьма характерно образование комплексов - радикалов. В обеих структурах атомы неметаллических элементов образуют радикалы С0з2 - в первом случае и S042 - - во втором. [17]
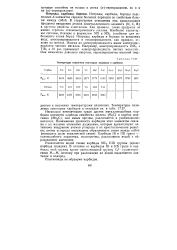 |
Температуры плавления некоторых нитридов и карбидов. [18] |
Нитриды, карбиды, бориды переходных d - элементов середин больших периодов по свойствам близки между собой. В структурном отношении они представляют продукты внедрения атомов неметаллического элемента ( N, С, В) в пустоты решеток cf - металлов. Как правило, такие продукты не имеют строгого стехиометрического состава. Нитриды, карбиды и бориды по внешнему виду, электропроводности и теплопроводности, как правило, похожи на металл. [19]
Наиболее важной из связей этого типа является ионная связь, обусловленная кулоновским притяжением избыточных электрических зарядов противоположно заряженных ионов. Атомы металлических элементов легко теряют свои внешние электроны; с другой стороны, атомы неметаллических элементов стремятся присоединить добавочные электроны. Таким образом, могут возникнуть стабильные анионы и катионы, которые могут в основном сохранить свои электронные структуры при приближении друг к другу и образовании стабильной молекулы или кристалла. [20]
При обыкновенной температуре все аллотропные видоизменения углерода химически инертны. При высоких температурах разрушаются их кристаллические решетки, освобождающиеся атомы становятся активными и легко вступают во взаимодействие с атомами металлических и неметаллических элементов. Графит более подвержен химическому воздействию, чем алмаз. [21]
В результате появляются многочисленные карбонитрыды, спликокар-биды, оксикарбонитриды и другие подобные соединения внедрения. На междоузлиях, так же как и па узлах, возможно образование упорядоченных структур, причем такие структуры могут быть образованы внедренными атомами и вакантными междоузлиями, играющими роль второго компонента при упорядочении. Узлы замещаются атомами металлов, а междоузлия - атомами неметаллических элементов. При этом концентрации атомов на той и другой подрешетке могут непрерывно изменяться в некоторых ( часто весьма широких) интервалах, а их чередование как на узлах, гак и на междоузлиях может характеризоваться появлением упорядоченных сверхетруктур. [22]
Установлено, что скорость диффузии в сплаве тем больше, чем / меньше атомный диаметр растворенного элемента. Например, атомы неметаллических элементов С, N, О, Н, диаметр которых меньше атомного диаметра железа, диффундируют в железо быстрее, чем атомы металлов. Поэтому температура, при которой про -; текает диффузия атомов неметаллических элементов, значительно) ниже температуры диффузии атомов металла; энергия активации при этом в несколько раз меньше. Скорость диффузии элемента находится в обратной зависимости от растворимости его в основном металле; она тем больше, чем дальше элементы расположены в периодической системе элементов Менделеева. [23]
Благодаря тому что электроны принадлежат одновременно двум атомам, каждый атом водорода приобретает структуру гелия, каждый атом углерода - структуру неона и каждый атом хлора - структуру аргона. Структуры этих молекул на бумаге представляют в одной плоскости, однако следует помнить, что октеты атомов имеют тетраэдрическое строение. Другие электронные структуры молекул, содержащих ковалентные связи, можно легко записать, если помнить о том, что следует заполнить октет атомов неметаллических элементов. [24]
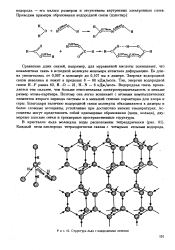 |
Структура льда с водородными связями. [25] |
Энергия водородной связи невелика и лежит в пределах 8 - 80 кДж / моль. Водородная связь проявляется тем сильнее, чем больше относительная электроотрицательность и меньше размер атома-партнера. Поэтому она легко возникает с атомами неметаллических элементов второго периода системы и в меньшей степени характерна для хлора и серы. Благодаря наличию водородной связи молекулы объединяются в димеры и более сложные ассоциаты, устойчивые при достаточно низких температурах. Ас-социаты могут представлять собой одномерные образования ( цепи, кольца), двумерные плоские сетки и трехмерные пространственные структуры. [26]
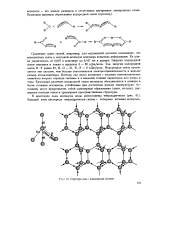 |
Структура льда с водородными связями. [27] |
Сравнение длин связей, например, для муравьиной кислоты показывает, что ковалентная связь в исходной молекуле мономера испытала деформацию. Энергия водородной связи невелика и лежит в пределах 8 - 80 кДж / моль. Водородная связь проявляется тем сильнее, чем больше относительная электроотрицательность и меньше размер атома-партнера. Поэтому она легко возникает с атомами неметаллических элементов второго периода системы и в меньшей степени характерна для хлора и серы. Благодаря наличию водородной связи молекулы объединяются в димеры и более сложные ассоциаты, устойчивые при достаточно низких температурах. Ас-социаты могут представлять собой одномерные образования ( цепи, кольца), двумерные плоские сетки и трехмерные пространственные структуры. [28]
Сравнение длин связей, например для муравьиной кислоты, показывает, что ковалентная связь в исходной молекуле мономера испытала деформацию. Большее или меньшее удлинение связи п - X и ее разрыхление наблюдается и в других веществах. Y упрочняет водородную связь. Энергия этой связи примерно в 10 раз больше энергии ван-дер-ваальсбвого взаимодействия и на порядок меньше энергии ковалентной связи. Водородная связь проявляется тем сильнее, чем больше относительная электроотрицательность и меньше размер атома-партнера. Поэтому она легко возникает с атомами неметаллических элементов второго периода Периодической системы и в меньшей степени характерна для хлора и серы. Несмотря на малую прочность водородной Связи, она определяет иногда структуру вещества и существенно влияет на его физические и химические свойства. Благодаря водородным связям молекулы объединяются в димеры и более сложные ассоциаты, устойчивые при достаточно низких температурах. [29]
Страницы: 1 2