Атом - первый элемент
Cтраница 1
Атом первого элемента в периодической системе - водорода - обладает наипростейшим строением. Оп состоит всего из двух частиц: протона и электрона, между которыми существуют лишь силы притяжения. Не случайно именно для атома водорода оказалась успешно применимой первая квантовая теория - теория Бора - и только для этого атома волновое уравнение Шредингера имеет точгное решение. [1]
Атом первого элемента в Периодической системе - водорода - обладает наипростейшим строением. Он состоит всего из двух частиц: протона и электрона, - между которыми существуют лишь силы притяжения. Не случайно именно для атома водорода оказалась успешно применимой первая квантовая теория - теория Бора, и только для этого атома волновое уравнение Шредингера имеет точное решение. [2]
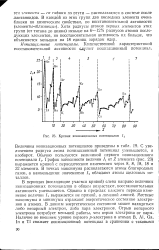 |
Кривая ионизационных потенциалов 1г. [3] |
Хотя радиусы атомов первых элементов этих групп ( от титана до цинка) меньше на 6 - 12 % радиусов атомов последующих элементов, но восстановительная активность их больше, что объясняется меньшим на 18 единиц зарядом ядер. [4]
 |
Последовательность расположения молекулярных орбиталей в гомо-нуклеарной молекуле. [5] |
Разность энергий 2s - и 2р - состояний в атомах первых элементов периодической системы приведена ниже. [6]
 |
Структурный тип NiAs.| Структурный тип BN. [7] |
Атомы второго элемента располагаются в тех же трех, уже занятых атомами первого элемента, тригональных призмах и на: всех вертикальных ребрах примитивных параллелепипедов. Они занимают такие положения в структуре, что оказываются на равных расстояниях от четырех ближайших атомов первого элемента. Все положения, занятые атомами каждого элемента, составляют одну правильную систему точек. [8]
В простейшем случае, когда один из образующих соединение элементов одновалентен, валентность второго элемента непосредственно указывает, сколько атомов первого элемента приходится на один атом второго в молекуле данного соединения. [9]
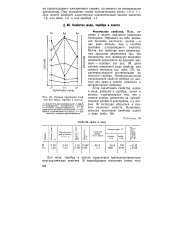 |
Кривые изменения свойств для меди, серебра и золота. [10] |
Если сопоставить свойства калия и меди, рубидия и серебра, цезия и золота, отличающихся тем, что у атомов первых элементов на предпоследнем уровне 8 электронов, а у вторых 18, нетрудно убедиться в резком различии свойств. [11]
При взаимодействии атомов двух элементов, из которых один находится в I, группе периодической системы, а другой - в VII группе, происходит отдача 1 электрона атомом первого элемента и присоединение этого электрона атомом другого элемента. [12]
Атомы первых элементов периодов имеют на внешнем уровне по одному s - электрону ( незавершенные внешние уровни) и потому проявляют сходные свойства - легко отдают валентные электроны, что обусловливает их металлический характер. [13]
Атомы первых элементов периодов имеют на внешнем уровне по одному s - электрону ( незавершенные внешние уровни) и потому проявляют сходные свойства - легко отдают валентные электроны, что обусловливает их металлический характер. [14]
 |
Структурный тип NaCl [ IMAGE ] Структурный тип CsCl. [15] |
Страницы: 1 2