Атом - электроотрицательный элемент
Cтраница 3
За счет иона водорода возможно возникновение довольно прочной связи между полярными молекулами типа ИХЭУ, где Э - атом электроотрицательного элемента: F, О, Cl, N и др. Подобную связь называют водородной. При такой связи ион водорода одной молекулы взаимодействует с электроотрицательным атомом другой по схеме: - Э Н -, где черта символизирует внутримолекулярную химическую связь, а отточием обозначена межмолекулярная водородная связь. [31]
Для аргона и неона известны только неустойчивые эксимер-ные соединения, например ArF и NeF, которые они образуют с атомами электроотрицательных элементов в электрическом разряде или под действием пучка электронов. Эксимерные соединения благородных газов применяют в газовых лазерах. [32]
Молекулы воды обладают способностью к образованию водородной связи не только между собой, но и с другими молекулами, содержащими атомы сильно электроотрицательных элементов. При таком взаимодействии молекулы воды могут через свой водородный атом связываться с наиболее отрицательными атомами других молекул или, наоборот, связываться с водородным атомом другой молекулы, если он несет достаточно высокий положительный заряд, усиливая этим полярность его связи с молекулой. Поэтому в этиловом спирте хлористый водород диссоциирует в сильной степени, а в динитробензоле в очень слабой, хотя диэлектрические проницаемости этих растворителей различаются лишь незначительно. [33]
 |
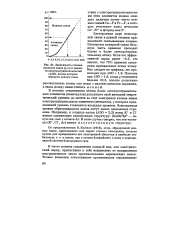
Зависимость степени ион-ности связи ( q / e от разности элек-троотрицательностей элементов ( Ах, атомы которых образуют данную связь. [34] |
В ионных соединениях атомы более электроотрицательных элементов ( неметаллов) дополняют свой внешний электронный слой до октета за счет электронов атомов менее электроотрицательных элементов ( металлов), у которых предвнешний слой становится внешним слоем. Электронные слои образовавшихся ионов могут иметь одинаковое строение. В этом случае говорят / что эти частицы ( К, С1 -, Аг) имеют изоэлектронную структуру. [35]
 |
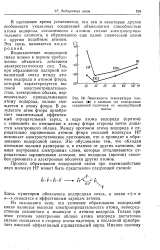
Зависимость степени ионности связи ( q / e от разности электроотрицательностей ( ДЭО, атомы которых образуют данную связь. [36] |
В ионных соединениях атомы более электроотрицательных элементов ( неметаллов) дополняют свой внешний энергетический уровень до октета за счет электронов атомов менее электроотрицательных элементов ( металлов), у которых пред-внешний уровень становится внешним уровнем. Электронные уровни образовавшихся ионов могут иметь одинаковое строение. Например, в хлориде калия ( ДЭО 2 2) ионы К и С1 - имеют одинаковую электронную структуру: ( Ne) 3s23p6 - такую же, как у атомов Аг. В этом случае говорят, что эти частицы ( К, С1 -, Аг) имеют изоэлектронную структуру. [37]
 |
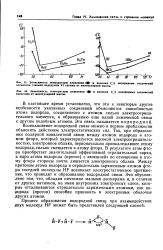
Зависимость температуры плавления ( и кипения ( о водородных соединений галогенов от молекулярной массы. [38] |
В настоящее время установлено, что эти и некоторые другие особенности указанных соединений объясняются способностью атома водорода, соединенного с атомом сильно электроотрицательного элемента, к образованию еще одной химической связи с другим подобным атомом. Эта связь называется водородной. [39]
 |
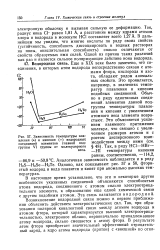
Зависимость температуры плавления ( я кипения ( О водородных соединений галогенов от молекулярной массы. [40] |
В настоящее время установлено, что эти и некоторые другие особенности указанных соединений объясняются способностью атома водорода, соединенного с атомом сильно электроотрицательного элемента, к образованию еще одной химической связи с другим подобным атомом. Эта связь называется водородной. [41]
Субкомплексные - это такие соединения, в которых атом наиболее электроположительного элемента различно ( по характеру связи) соединен с атомами разных электроотрицательных элементов, или такие соединения, в которых атом наиболее электроотрицательного элемента различно связан с атомами разных электроположительных элементов. [42]
 |
Зависимость температуры пла - г, . [43] |
В настоящее время установлено, что эти и некоторые другие особенности указанных соединений объясняются способностью атома водорода, соединенного с атомом сильно электроотрицательного элемента, к образованию еще одной химической связи с другим подобным атомом. Эта связь называется водородной. [44]
Субкомплексные - это такие соединения, в которых атом наиболее электроположительного элемента различно ( по характеру связи) соединен с атомами разных электроотрицательных элементов, или такие соединения, в которых атом наиболее электроотрицательного элемента различно связан с атомами разных электроположительных элементов. [45]
Страницы: 1 2 3 4