Взаимодействующий атом
Cтраница 3
Между разностью электроотрицательностей взаимодействующих атомов и сдвигом электронного облака существует прямая зависимость. [31]
Перекрывание таких орбиталей взаимодействующих атомов, как указывалось в предыдущем параграфе, неэффективно, так как число электронов на образующихся связывающих и разрыхляющих МО одинаково. [32]
При большом числе взаимодействующих атомов имеются электронные орбитали, энергии которых примерно равны энергии электронных орбиталей в изолированных атомах. [33]
При одинаковой электроотрицательности взаимодействующих атомов выигрыша энергии при переходе электрона не происходит и, следовательно, имеются условия для образования валентной связи. [34]
В случае, когда взаимодействующие атомы имеют близкие или одинаковые значения электроотрицательности, связь между ними может осуществляться вследствие совместного пользования парой электронов. Электроны с орбиты одного из атомов переходят на совместную орбиту двух атомов; образуемая та - - 1аии - образом С1ягзБ - - атимии носит название ковалентной. [35]
При образовании ионной связи взаимодействующий атом передает другому один или большее количество электронов, в результате чего атомы превращаются в ионы противоположного знака. Притягиваясь друг к другу, ионы образуют нейтральную молекулу. [36]
Фазовое пространство Г системы взаимодействующих атомов делится так называемой критической поверхностью S на ряд областей, которые отождествляются с участками пространства, отвечающими различным стабильным молекулярным образованиям. [37]
Эффект искажения для системы взаимодействующих атомов автоматически учитывается в хартри-фо-ковских расчетах, основывающихся на молекулярных орбиталях самосогласованного поля. Притяжение при больших г является межоболочечным корреляционным эффектом. [38]
Если один из пары взаимодействующих атомов в достаточной мере электроположителен, а другой - электроотрицателен, то первый атом может передать валентный электрон второму атому, вследствие электростатического ( кулоновского) взаимодействия противоположно заряженных ионов возникает сила притяжения и образуется ионная связь. [39]
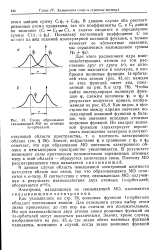 |
Схема образования. [40] |
Для этого расположим ядра взаимодействующих атомов на том расстоянии друг от друга ( г), на котором они находятся в молекуле, и изобразим волновые функции ls - орбита-лей этих атомов ( рис. 43, а); каждая из этих функций имеет вид, показанный на рис. 9, а ( стр. [41]
Для этого расположим ядра взаимодействующих атомов на том расстоянии друг от друга ( г), на котором они находятся в молекуле, и изобразим волновые функции ls - орбиталей этих атомов ( рис. 43, а); каждая из этих функций имеет вид, показанный на рис. 9, а ( стр. Как видно, в пространстве между ядрами значения молекулярной волновой функции if больше, чем значения исходных атомных волновых функций. Значит, возрастание я л в сравнении с tyi и г) 2 означает, что при образовании МО плотность электронного облака в межъядерном пространстве увеличивается. В результате возникают силы притяжения положительно заряженных атомных ядер к этой области - образуется химическая связь. [42]
Для этого расположим ядра взаимодействующих атомов на том расстоянии друг от друга ( г), на котором они находятся в молекуле, и изобразим волновые функции ls - орбиталей этих атомов ( рис. 43, а); каждая из этих функций имеет вид, показанный на рис. 9, а ( стр. Как видно, в пространстве между ядрами значения молекулярной волновой функции ty больше, чем значения исходных атомных волновых функций. Значит, возрастание i) в сравнении с to и to означает, что при образовании МО плотность электронного облака в межъядерном пространстве увеличивается. В результате возникают силы притяжения положительно заряженных атомных ядер к этой области - образуется химическая связь. Поэтому МО рассматриваемого типа называется связывающей. [43]
Для этого расположим ядра взаимодействующих атомов на том расстоянии друг от друга ( г), на котором они находятся в молекуле, и изобразим волновые функции ls - орбиталей этих атомов ( рис. 43, а); каждая из этих функций имеет вид, показанный на рис. 9, а ( стр. Как видно, в пространстве между ядрами значения молекулярной волновой функции больше, чем значения исходных атомных волновых функций. Значит, возрастание ч) в сравнении с ty и 1) з2 означает, что при образовании МО плотность электронного облака в межъядерном пространстве увеличивается. В результате возникают силы притяжения положительно заряженных атомных ядер к этой области - образуется химическая связь. Поэтому МО рассматриваемого типа называется связывающей. [44]
Для этого расположим ядра взаимодействующих атомов на том расстоянии друг от друга ( г), на котором они находятся в молекуле, и изобразим волновые функции ls - орбиталей этих атомов ( рис. 43, а); каждая из этих функций имеет вид, показанный на рис. 9, а ( стр. Как видно, в пространстве между ядрами значения молекулярной волновой функции з больше, чем значения исходных атомных волновых функций. [45]
Страницы: 1 2 3 4