Креатинкиназа
Cтраница 1
Креатинкиназа ( АТФ: креатинфосфотрансфераза, КФ 2.7.3.2) катализирует обратимый перенос фосфорильной группы от АТФ к креатину. [1]
Креатинкиназа - фермент, принимающий участие в энергетическом обмене клеток мышечной, нервной и других тканей. Повышение активности креатинкиназы наблюдается при повреждении миокарда ( инфаркт миокарда, миокардит), мышечной ткани ( травма, мышечные дистрофии, дерматомиозит, полимиозит и др.), при обширных оперативных вмешательствах, тяжелой физической нагрузке, внутримышечных инъекциях лекарственных средств ( особенно наркотических и обезболивающих), гипотиреозе, острой алкогольной интоксикации. [2]
Креатинкиназа выходит в свободном объеме колонки при элюции этим же буфером, тогда как примеси связываются с ДЭАЭ-целлюлозой. [3]
Подобно креатинкиназе аргининкиназа, по-видимому, подчиняется кинетике быстрого статистического равновесия. Сообщение [72] о том, что у фермента из Jasus verrauxi реакция имеет механизм типа пинг-понг, не содержало достаточно убедительных доказательств. Хотя и имеются некоторые количественные различия, однако характер усиления релаксации одинаков во всех случаях, а константы диссоциации комплексов марганца с нуклеотидами, определенные по скоростям релаксации протонов, хорошо согласуются со значениями, полученными из кинетических данных. [4]
С открытием митохондриальной креатинкиназы креатинфосфаг стал рассматриваться не просто как резерв макроэргического фосфата в клетке, а как основной переносчик химической энергии от митохондрий к местам ее утилизации в клетке. Митохондриальная креатинкиназа превращает синтезированный в митохондриях АТФ в креатинфос-фат; в виде креатинфосфата энергия транспортируется к местам ее утилизации, где и происходит обратная реакция образования АТФ из креатинфосфата и АДФ с помощью цитоплазматических изоферментов. [5]
Некоторые сведения о природе этих изменений получены в начальных работах со спин-меченой креатинкиназой. [6]
Моррисону и Джеймсу [2] принадлежит отличное исследование механизма с образованием тройного комплекса для реакции, катализируемой креатинкиназой. [7]
Ферментами, особенно специфичными для мышечной ткани ( скелетной и сердечной), являются, в частности, креатинкиназа, катализирующая образование фосфокреатина из креатина и АТФ, дегидрогеназа Р - ОКСИ-масляной кислоты ( р-оксибутиратдегидрогеназа) и некоторые другие. Определение этих ферментов приобретает особый интерес при инфаркте миокарда и при различных миопатиях. При заболеваниях печени в плазме крови появляется гистидаза. [8]
На данной стадии исследований представляется, что аргининкиназа и, вероятно, другие гуанидинкиназы [74, 75] имеют механизм, подобный креатинкиназе. Гораздо меньшая молекулярная масса аргининкиназы делает ее более удобной для изучения методом сканирующей ЯМР-спектроскопии. [9]
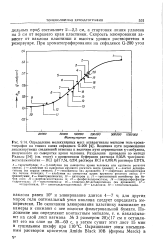
С; 11 - трипсиновый ингибитор ( из бобов сои); 12 - - карбоксипептидаза А; 13 - фосфоглицеромутаза; 14 - глицеролфосфатде-гндрогеназа; 15 - креатинкиназа; 16 - глицерол-б Р - дегидрогеназа ( из дрожжей); 17 - аспарагиназа; 18 - алкогольдегидрогеназа; 19 - альдолаза; 20 - глюкозоксидаза. [11]
С открытием митохондриальной креатинкиназы креатинфосфаг стал рассматриваться не просто как резерв макроэргического фосфата в клетке, а как основной переносчик химической энергии от митохондрий к местам ее утилизации в клетке. Митохондриальная креатинкиназа превращает синтезированный в митохондриях АТФ в креатинфос-фат; в виде креатинфосфата энергия транспортируется к местам ее утилизации, где и происходит обратная реакция образования АТФ из креатинфосфата и АДФ с помощью цитоплазматических изоферментов. [12]
По данным И. П. Тюриной ( 1976), начиная с 1 - х суток после лучевого воздействия и на протяжении длительного времени, острое лучевое поражение у людей характеризуется существенными изменениями активности органоспецифических ферментов сыворотки крови. Повышение активности креатинкиназы в сыворотке крови свидетельствует не столько об общем поражении организма, сколько о действии локальных доз на скелетные мышцы. [13]
Креатинкиназа - фермент, принимающий участие в энергетическом обмене клеток мышечной, нервной и других тканей. Повышение активности креатинкиназы наблюдается при повреждении миокарда ( инфаркт миокарда, миокардит), мышечной ткани ( травма, мышечные дистрофии, дерматомиозит, полимиозит и др.), при обширных оперативных вмешательствах, тяжелой физической нагрузке, внутримышечных инъекциях лекарственных средств ( особенно наркотических и обезболивающих), гипотиреозе, острой алкогольной интоксикации. [14]
В настоящее время известно много различных ферментов, существующих в виде различных форм. Это малатдегидрогеназа, креатинкиназа, щелочная фосфатаза, изо-мераза глюкозо-6 - фосфата и др. По строению все исследованные изоферменты одного фермента отличаются друг от друга разными соотношениями различных полипептидных цепей. [15]
Страницы: 1 2 3