Креатинкиназа
Cтраница 2
Иная возможность заключается в одновременном, кооперативном действии активных групп фермента; наличие я-электронного сопряжения или иных форм взаимного влияния атомов в молекуле субстрата облегчает эффект одновременного действия активных групп фермента на молекулу субстрата. Примером может служить фосфорилирование креатина креатинкиназой. [16]
А - Н RO - Р0д - - АРОз - ROH, протекают, по-видимому, по этому механизму. Хорошим примером таких ферментов может служить креатинкиназа. [17]
Размер повреждения миокарда при возникновении ишемии, снижение активности ферментов в сердечной мышце и возрастание активности соответствующих ферментов в сыворотке крови ( например, креатинкиназы) в значительной мере коррелируют друг с другом. Следует признать, что в диагностике инфаркта миокарда определение активности креатинкиназы, Ac AT и ЛДГ в сыворотке крови-наиболее чувствительные тесты. Повышение активности указанных ферментов, особенно креатинкиназы, является постоянным и наиболее высоким. В последние годы четко показано, что определение в сыворотке крови миокардиально специфичных белков ( миоглобин, тро-понин Т и др.) - весьма чувствительный ранний тест повреждения миокарда. [18]
Ткани, имеющие большой динамический диапазон энергетического обмена ( скелетная и сердечная мышцы), а также мозг содержат креа-тинкиназу ( с. Во внутренней мембране митохондрий скелетных мышц, сердца и мозга содержится креатинкиназа, отличная по элект-рофоретической подвижности и термолабильности от трех изофермен-тов креатинкиназы цитоплазмы. Активность креатинкиназы в митохондриях достаточна для того, чтобы в присутствии избытка креатина обеспечить превращение всего образующегося в процессе окислительного фосфорилирования АТФ в креатинфосфат. Освобождающийся при этом АДФ вновь фосфорилируется в митохондриях. Таким образом, высокая активность креатинкиназы в митохондриях может поддерживать работу дыхательной цепи на постоянно высоком уровне в тканях, лишь периодически испытывающих потребность в большом количестве АТФ. [19]
Глю-козо - 6-фосфатдегидрогеназа, о-глицеральдегид - З - фосфатдегидро-геназа и миокиназа связывались только Р - ( 6-аминогексил) - Р2 - ( 5 -аденозин) пирофосфат - сефарозой, в то время как алкоголь-дегидрогеназа и глицерокиназа связывались только № - ( 6-амино-гексил) - 5 - АМР - сефарозой. Лактатдегидрогеназа, малатдегидро-геназа, 3-фосфоглицераткиназа и пируваткиназа связывались обоими сорбентами, а гексокиназа и креатинкиназа не связывались ни одним из них. Эти результаты отражают природу фермент-нук-леотидных взаимодействий; можно сделать вывод, что в то время как свободная 5 -фосфатная группа существенна для связывания, например, алкогольдегидрогеназы или глидерокиназы, она играет совершенно другую роль при взаимодействии с глицеральдегид-3 - фосфатдегидрогеназой. В этом случае решающая роль принадлежит аденозиновой части аффинанта. [20]
Выше уже рассматривались результаты кинетических исследований фермента ( разд. Мы не будем обсуждать работы группы Куби [66] и других лабораторий [68, 69], посвященные белковой химии креатинкиназы. Основное внимание будет уделено лишь тем сведениям, которые были получены методом магнитного резонанса, а также при параллельных исследованиях. [21]
Было также высказано предположение о том, что именно креатинфосфат является той формой высокоэргического фосфата, которая переносится из митохондрий в другие части клетки. В настоящей работе предлагается ознакомиться с влиянием креатина на дыхание митохондрий сердца и определить 50s митохондриальной креатинкиназы для креатина и АТФ. [22]
В мозговой ткани содержится большое количество ферментов, катализирующих обмен углеводов, липидов и белков. До сих пор в кристаллическом виде из ЦНС млекопитающих выделены лишь некоторые ферменты, в частности ацетилхолинэстераза и креатинкиназа. [23]
Весьма важно, что после инфаркта миокарда уже в первые часы в крови резко увеличивается активность фермента креатин-киназы, характерного для мышечной ткани. Если скелетная мускулатура у больного нормальна и у него подозревается инфаркт миокарда, то появление и быстрый рост активности креатинкиназы в крови может служить решающим диагностическим признаком, более убедительным, чем, например, показатели электрокардиограммы. Лишь позднее начинает изменяться в крови содержание трансаминазы, и еще позже - лактикодегидрогеназы. [24]
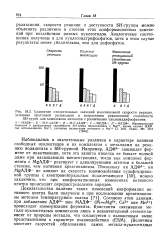 |
Сравнение относительных значений максимальной скорости реакции. [25] |
Например, АДФ3 - защищает фермент от инактивации, хотя эта защита никогда не бывает полной даже при насыщающих концентрациях, тогда как комплекс фермента с М АДФ - реагирует с алкилирующим агентом в большей степени, чем нативная креатинкиназа. Поскольку ни АДФ3 - -, ни Л АДф - не влияют на скорость взаимодействия сульфгидриль-ной группы с электронейтральным иодацетамидом [50], можно заключить, что при конформационных изменениях активного центра происходит перераспределение зарядов. [26]
Было показано, что для этой реакции величина AG при рН 7 4, температуре 30 С и в присутствии 0 01 М Mg2 равна 2 8 ккал / моль. Хотя направление изменения свободной энергии не способствует синтезу креатинфосфата в стандартных условиях, тем не менее при накоплении АТФ в отдыхающих мышцах реакция будет смещаться в правую сторону, благодаря чему высокоэнергетический фосфат будет запасаться до тех пор, пока он не понадобится. Креатинкиназа была открыта в 1935 г. Лох-манном, который до этого открыл АТФ. [27]
КИНАЗЫ, фосфотрансфера-з ы, ферменты класса трансфераз, катализирующие реакции переноса фосфо-рильного остатка ( - РО3Н2) от АТФ ( реже - от др. нуклеозидтрифосфатов) на разл. Определение активности креатинкиназы в сыворотке крови используют в диагностике инфаркта миокарда, миопатий. [28]
Некоторая информация была получена методом ЭПР. Спектры ЭПР очень чувствительны к напряженности поля около иона металла и, следовательно, к любым изменениям его лигандов. При связывании МпАДФ - с креатинкиназой [34, 35] и МпАТФ2 - с аденилаткиназой [36] не обнаружено никаких изменений в спектрах ЭПР. Эти данные подтверждают ( хотя и не доказывают) гипотезу о том, что в растворе, как и на ферменте, структура комплексов одинакова. [29]
Она широко распространена среди беспозвоночных, особенно у членистоногих. Ферменты, выделенные из некоторых ракообразных, почти не отличаются друг от друга по физическим свойствам. Аргининкиназа состоит из одной полипептидной цепи с молекулярной массой около 40 000 ( половина молекулярной массы креатинкиназы) с одним каталитическим центром. [30]
Страницы: 1 2 3