Кревелен
Cтраница 1
Кревелен и Гофтейзер [4], изучавшие образование пузырей в системе воздух-вода на стеклянных соплах, направленных кверху, отмечают затруднения, с какими они встретились, когда диаметр капилляров был больше 3 мм, вследствие внутреннего смачивания, которое они рекомендуют устранять применением внутреннего парафинового покрытия. [1]
 |
К определению афиз. и ахим. [2] |
Кревелен объясняют тем, что при физической абсорбции часть поверхности насадки, покрытая медленно обновляющейся застойной жидкостью, не активна; при хемосорбции в условиях независимости массоотдачи от гидродинамического режима активна вся смоченная поверхность насадки. [3]
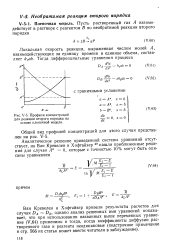 |
Профили концентраций. [4] |
Ван Кревелен и Хофтайзер привели результаты расчетов для случая DA DB, однако анализ решенных ими уравнений показывает, что при использовании названных выше переменных уравнение (V.64) применимо и тогда, когда коэффициенты диффузии растворенного газа и реагента неодинаковые ( подстрочное примечание к стр. [5]
Ван Кревелен и Хофтайзер 122 предложили для этого случая графический метод. [6]
 |
Давление паров эфира.| Давление паров эфира над растворами в различных растворителях ( Robinson, Recovery of Volatile Solvents, New York, 1922. [7] |
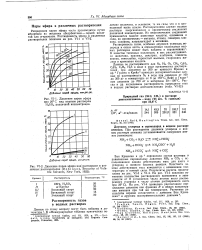
Ван Кревелен и др. 5 определили состав раствора и равновесные парциальные давления NH3 и СО2 с использованием закона действующих масс для азота и углерода и ионного баланса реакции. Константа закона действующих масс изменяется с изменением температуры и ионной силы. Результаты расчета представлены на рис. VI-3 и VI-4. На рис. VI-4 приведено рассчитанное парциальное давление как функция R и общая концентрация аммиака при той же температуре. [8]
Ван Кревелен и Хофтицер [102] на основе пленочной модели разработали метод численного интегрирования, а также приближенное решение. [9]
Ван Кревелен и Хофтайзер 122 предложили для этого случая графический метод. [10]
Ван Кревелен разработал также метод инкрементов для расчета КО, исходя из строения полимера. [11]
Ван Кревелен, правда, не учитывал изменения концентрации в продольном направлении, но это оправдано в простейшем случае потока вещества от бесконечной плоскости г / 0 в полупространство yQ над плоскостью. [12]
Ван Кревеленом и Хофтайзером, данные о растворимостях. [13]
Марс и Ван Кревелен [118,119] изучили влияние парциального давления бензола на скорость окисления бензола в небольшом псевдоожи-женном слое катализатора. [14]
Марс и Ван Кревелен сообщают, что их данные соответствуют интегрированной форме уравнения ( 5), однако не указывают, каковы степени превращения, при которых они получили эти данные. [15]
Страницы: 1 2 3 4 5