Индивидуальный атом
Cтраница 3
Уже довольно давно известно, что большинство свойств сравнительно сложных молекул можно представить в виде суммы соответствующих вкладов индивидуальных атомов или связей. Физически подобные эмпирические закономерности основаны на том, что силы химической связи между атомами внутри молекулы или между атомами различных молекул проявляются на расстоянии 0 1 - 0 3 нм. [31]
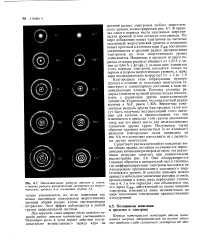 |
Относительные радиусы атомов и ионов, а также радиусы распределений электронов на энергетических уровнях для элементов группы IA. [32] |
Благородные газы ( образующие нулевую группу) в отличие от остальных неметаллов существуют в элементарном состоянии в виде индивидуальных атомов. [33]
Дж, кДж) - это та энергия, которая выделяется при образовании кристалла из бесконечно разреженного газа индивидуальных атомов. Энергии атомизации отвечает химический процесс лМ ( г) / пА ( г) - ( М Ат) ( г) - Еет. [34]
Он отражает не только межвидовые, но и межподвидо-вые генетические связи атомов, показывая процесс взаимопревращения на уровне индивидуальных атомов. Но, скопировав матрицу с таблицы химических элементов, ученые стеснили себя в свободе варьирования переменными. Они трактовали закон смещений только применительно к превращениям химических элементов ( видов атомов) друг в друга. Это обстоятельство и привязало их к клеткам таблицы, где минимальным шагом смещения является ход от клетки к клетке, что равнозначно - от химического элемента к химическому элементу. Так, исподволь, из процесса систематизации химических элементов вычленяется новый объект систематизации - атом. [35]
Различные уже известные нам факты свидетельствуют о том, что во многих молекулах электроны не локализованы между двумя индивидуальными атомами. Теория молекулярных орби-талей также исходит из того, что электроны распределяются вдоль всей молекулы, и эти предположения ограничиваются в основном свойствами симметрии молекулы и энергией электронов. [36]
Хотя механическая модель атома или молекулы не может быть четко определена, математические законы, определяющие свойства и поведение индивидуальных атомов и молекул, теперь твердо установлены с помощью квантовой механики. [37]
Сегодня же мы предпочитаем обозначать через р полную плотность зарядов, включая в нее и заряды, связанные с индивидуальными атомами. [38]
Поэтому химические символы элементов обычно соответствую ют одному молю ( 6 0225 - 1023) атомов, а также обозначают индивидуальные атомы или молекулы. [39]
 |
Распределение потенциала ядра ф и потенциала электронной оболочки ср атома водорода ( проекция.| Искажение формы. [40] |
Обсуждая эти результаты, следует иметь в виду вообще некоторую произвольность представления о разделении электронной плотности молекулы на электронные плотности индивидуальных атомов и связей. [41]
Почему же металлы, и прежде всего такие, как медь, серебро, золото, имеют обобществленные электроны, легко покидающие индивидуальный атом. [42]
Уже довольно давно химикам и физикам стало известно, что большинство свойств сравнительно сложных молекул можно представить в виде суммы соответствующих вкладов индивидуальных атомов или связей. Физически подобные эмпирические закономерности основаны на том, что силы, действующие между атомами внутри молекулы или между атомами различных молекул, являются очень близкодействующими. Силы эти действуют на расстояниях 1 - 3 А. [43]
 |
Термограмма ZrHi92 при нагревании в аргоне. [44] |
Нейтронографичеокое изучение гидридов ZrH [325] и ZrHi & [326] позволило установить в их спектрах термических вибраций частоты, соответствующие примерно частотам вибрации индивидуальных атомов водорода. [45]
Страницы: 1 2 3 4