Диаграмма - энергия
Cтраница 1
Диаграмма энергий на рис. 13, строго говоря, применима только для одноэлектронного случая. [1]
 |
Энергетическая диаграмма, иллюстрирующая различие между кинетическим и термодинамическим контролем за количеством образующихся туатомеров при ассоциации ионов, а также раз. [2] |
Диаграмма энергий, приведенная на рис. 50, поясняет изложенное выше. [3]
Диаграмма энергии МО для молекулы А-В ( рис. 137) показывает, что энергия als молекулярной орбитали близка к энергии Is АО атома В. [4]
Диаграмма энергии МО для молекулы АВ ( рис. 4.20) показывает, что энергия о Is молекулярной орбитали близка к энергии Is АО атома В. [5]
На диаграмме энергии ( см. рис. XI.1) это состояние должно соответствовать седловинной точке гиперповерхности энергии. [6]
На диаграмме энергии МО, изображенной на рис. 118, величины а и с зависят от степени перекрывания АО разнородных атомов и являются мерой... [7]
Ниже приведены диаграммы энергий орбиталеи монооксидов азота и углерода. Объясните с помощью этих диаграмм, почему N0 парамагнитен, а СО нет. [8]
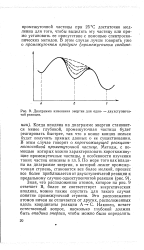 |
Диаграмма изменения энергии для одно - - двухступенчатой реакции. [9] |
Когда впадина на диаграмме энергии становится менее глубокой, промежуточная частица будет реагировать быстрее, так что в конце концов нельзя будет получить прямых данных о ее существовании. [10]
 |
Сплошной спектр излучения столба дуги в сравнении с солнечным спектром ( Е. Ролласон, Е. Ван-Сом - мерн. [11] |
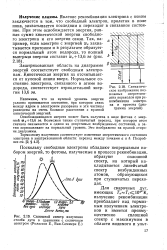
Заштрихованная область на диаграмме энергий соответствует свободным электронам. Кинетическая энергия их отсчитывается от нулевой линии вверх. [12]
Заштрихованная область на диаграмме энергий соответствует свободным электронам. Кинетическая энергия их отсчитывается от нулевой линии вверх. Нормальное состояние, электрона, связанного в атоме водорода, соответствует отрицательной энергии 13 6 эв. [14]
На рис. 136 показана диаграмма энергии МО для молекулы водорода. [15]
Страницы: 1 2 3