Любой атом
Cтраница 2
Любой атом пара может сконденсироваться в любом месте стенки сосуда и на любой стороне экрана; наличие или отсутствие экрана внутри сосуда практически не сказывается на характере движения молекул, никакой молекулярной тени на стенке сосуда за экраном не получается. [16]
Поскольку любой атом с равной вероятностью может начать излучать в любой момент времени t, то среднее число цугов, начало которых приходится на любой малый интервал времени At равно n N At / то. [17]
Ядро любого атома также создает магнитный момент, однако он настолько мал, что не оказывает существенного влияния на магнитные свойства атома. Электроны вращаются вокруг ядра по определенным орбитам, образуя электронную оболочку атома. Электроны оболочки, количество которых равно порядковому номеру элемента в таблице Менделеева, распределяются между подоболочками и электронными слоями. [18]
Для любого атома возможно столько потенциалов ионизации, сколько у него электронов. Потенциал ионизации характеризует способность атома терять свои электроны. Чем ниже потенциал ионизации, тем легче атом теряет свои электроны и тем сильнее у него выражены металлические свойства. Наименьшим потенциалом ионизации обладает цезий. [19]
Для любого атома, кроме атома водорода, задача нахождения собственных функций и собственных значений (11.14) не может быть решена точно. Наилучшим и в действительности единственным приближенным методом решения этой задачи является метод самосогласованного поля, предложенный Хартри и усовершенствованный Фоком. [20]
У любого атома в невозбужденном состоянии может быть одно значение орбитального радиуса и множество значений для возбужденных состояний. Радиусы атомов имеют максимальное значение в начале периода, а затем несколько уменьшаются при переходе слева направо. Это связано с последовательным увеличением заряда ядра и, соответственно, числа электронов. При переходе к новому периоду радиус вновь резко увеличивается, так как при этом появляется новый энергетический уровень. [21]
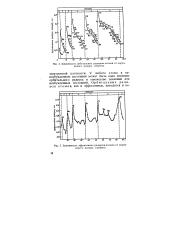 |
Зависимость орбитальных радиусов атомов от порядкового номера элемента.| Зависимость эффективных радиусов атомов от порядкового номера элемента. [22] |
У любого атома в невозбужденном состоянии может быть одно значение орбитального радиуса и множество значений для возбужденных состояний. [23]
Вместо любого атома водорода в этих структурах может иметься алкильная группа. Замещение у атома углерода на алкил еще больше усиливает стабилизацию образующегося иона; так, например, mpem - бутанол дает очень интенсивный пик с массой 59 и не образует пика с массой 74, отвечающего его молекулярному весу. Стабилизация этого типа усиливается, по-видимому, в порядке, обратном возрастанию электроотрицательности гетероатома, например: амины меркаптаны спирты. [24]
Вместо любого атома водорода в этих структурах может иметься алкильная группа. Замещение у атома углерода на алкил еще больше усиливает стабилизацию образующегося иона; так, например, ягреяг-бутанол дает очень интенсивный пик с массой 59 и не образует пика с массой 74, отвечающего его молекулярному весу. Стабилизация этого типа усиливается, по-видимому, в порядке, обратном возрастанию электроотрицательности гетероатома, например: амины меркаптаны ] спирты. [25]
К любому атому, входящему в состав кольца, или к нескольким таким атомам, можно присоединить еще один атом углерода или целую цепочку атомов, которые называют обычно боковыми цепями. [26]
В любом атоме орбитальный момент взаимодействует со спиновым. [27]
В любом атоме, вообще говоря, имеется несколько электронов, и его полный момент количества движения и полный магнитный момент представляют некоторую комбинацию спиновых и орбитальных моментов. И без каких-либо на то классических оснований в квантовой механике ( для изолированного атома) направление магнитного момента всегда противоположно направлению момента количества движения. Отношение их не обязательно должно быть - qjm или - qJ2m; оно расположено где-то между ними, ибо здесь перемешиваются вклады от спинов и орбит. [28]
В любом атоме существует ряд энергетических уровней. Нижние из них заполнены электронами, более высокие не заполнены, но могут принимать электроны с нижних уровней при возбуждении атома. Каждому из уровней электронов в решетке кристалла соответствует энергетическая зона. Одни зоны кристалла образуются путем уширения уровней катионов, другие - уровней анионов. При этом каждая из образующихся зон служит обобществленным уровнем всех катионов или всех анионов кристалла. Зазор между этими зонами соответствует тем значениям энергии, которые электрон не может получить в решетке кристалла. [29]
В любом атоме число орбиталей бесконечно. [30]
Страницы: 1 2 3 4