Свободный атом - кислород
Cтраница 2
Поэтому наличие сплошного спектра может считаться доказательством присутствия в зоне разряда свободных атомов кислорода, которые играют активную роль в процессе образования озона. [16]
Следовательно, озон может образовываться во всех физических и химических процессах, в результате которых возникают свободные атомы кислорода. [17]
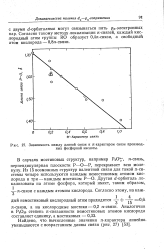 |
Зависимость между длиной связи и it - характером связи производи. [18] |
Согласно такому методу локализации я-связей, каждый кислородный атом группы RO образует 0 4л - связи, а свободный атом кислорода - 0 8я - связи. [19]
В этой реакции два активных центра приводят к образованию четырех - в виде двух радикалов ОН и двух свободных атомов кислорода с высокой реакционной способностью. [20]
Как было показано Налбандяном [53], введение малых количеств свободных атомов водорода, полученных в разрядной трубке, или свободных атомов кислорода, полученных фотохимическим путем непосредственно в реагирующей смеси, расширяет область воспламенения. [21]
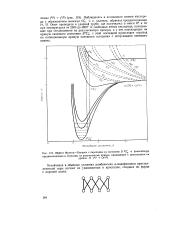 |
Эффект Франка-Кондона с переходом на состояние В 8SU и дальнейшую преддиссоциацию и переходы на репульсивные кривые, приводящие к диссоциации на. [22] |
Опыт проводили в ударной трубе, где получались в смеси О3 и Аг при температурах от 2500 до 3800 К свободные атомы кислорода, попадающие при столкновении на репульсивную кривую, а с нее переходящие на кривую связевого состояния Б32и; с этой последней происходит переход на потенциальную кривую основного состояния с испусканием светового кванта. [23]
В результате неподеленная пара ( 2ру) 2 атома кислорода испытывает со стороны других электронов большее отталкивание, чем в свободном атоме кислорода. Следовательно, потенциал ионизации этой пары должен понизиться по сравнению со значением, характерным для свободного атома, что и наблюдается на опыте. В то время как потенциал ионизации для свободного атома кислорода равен 13 5 эв, для формальдегида он равен только 11 эв. [24]
Некоторые авторы считают, что перманганат калия, взаимодействуя с парафином при 140 - 150, раскисляется до двуокиси марганца с выделением свободных атомов кислорода, которые, реагируя далее с углеводородами, образуют свободные углеводородные радикалы [1], участ-вующие в дальнейшем развитии процесса. [25]
 |
Структура серилфосфата 19 ]. [26] |
Оказывается, что силовая константа для растяжения связи Р - О уменьшается только для атомов кислорода, связанных с ионом - металла, а для свободных атомов кислорода она увеличивается, в результате чего средняя силовая константа связи Р - О остается неизменной. Похожим образом ведут себя другие оксианионы: сульфат, карбонат и нитрат. [27]
Как и при тренировке образца в вакууме, адсорбция сероводорода при комнатной температуре приводит к появлению в спектре полос поглощения 1160 и 1300 см 1, обусловленных симметричными и антисимметричными колебаниями связей серы со свободными атомами кислорода бидентатно связанных сульфатных комплексов. При увеличении температуры от 100 до 300 С наблюдается постепенное исчезновение этих полос поглощения и образование двух новых полос 1225 и 1360 см, которые относятся к органическим сульфатам. [28]
Как и при тренировке образца в вакууме, адсорбция сероводорода при комнатной температуре приводит к появлению в спектре полос поглощения 1160 и 1300 см 1, обусловленных симметричными и антисимметричными колебаниями связей серы со свободными атомами кислорода бидентатно связанных сульфатных комплексов. При увеличении температуры от 100 до 300 С наблюдается постепенное исчезновение этих полос поглощения и образование двух новых полос 1225 и 1360 см 1, которые относятся к органическим сульфатам. [29]
По поводу окисления индиго кислородом воздуха в присутствии водородистого палладия Траубе заметил, что Гоппе-Зейлер упустил из вида очень важный факт, а именно, что водород в момент выделения соединяется с кислородом, образуя перекись водорода, которая и могла произвести окисления, приписываемые Гоппе-Зейлером свободным атомам кислорода. [30]
Страницы: 1 2 3 4