Кривая - круговой дихроизм
Cтраница 3
Это новое правило справедливо только для я - я - перехода, но его можно применить и к наблюдаемому переходу при 330 ммк, ввиду того что, как мы увидим позднее, существует связь между знаками кривых кругового дихроизма, которые обусловлены этими двумя переходами. [31]
Эти вещества сильно поглощают в ультрафиолетовой области около 267 ммк, но проявляют также оптическую активность при 310 ммк. Кривые кругового дихроизма для гидантоинов, полученных из L-аланина и L-пролина [4], показаны на рис. 133 и 134 соответственно. Недостатком этих производных является довольно легкая рацемизация, но связь между знаком полосы при 310 ммк и конфигурацией точно такая же, как и для ди-тиокарбаматов. Используют их аналогичным образом. [32]
 |
Конфигурация и октантная диаграмма 17х - окси-20 - кетостероидов. [33] |
Водородная связь сдвигает п - л - переход карбонильной группы в сторону более коротких длин волн, и, следовательно, аналогичным образом изменяется круговой дихроизм рассматриваемых молекул. В целом кривая кругового дихроизма должна иметь форму суммарной кривой. Однако в действительности это не совсем так; если мы примем во внимание различие в амплитуде и величине батохромного сдвига, то увидим, что кривые кругового дихроизма 20-кетопрегнана совмещаются с кривыми кругового дихроизма соответствующих 17а - оксипроиз-водных. [34]
На основании нескольких приведенных примеров в настоящее время нельзя точно установить взаимосвязь между структурой и оптической активностью сопряженных карбоновых кислот. Однако, сравнивая кривые кругового дихроизма для пар соединений ( CLVIII и CLIX, CLXIII и CLXV, CLXIV и CLXVI), можно сделать предположение, что инверсия асимметрического центра в а-положении относительно двойной связи изменяет знак оптической активности. Однако пока еще не известно, будет ли изменяться знак, если в этом же положении находится иной заместитель, а не гидроксильная или ацетоксигруппа. [35]
Аквокобаламин можно считать слабым основанием; с кислотами он образует кристаллические соли. На основании большого сходства кривых кругового дихроизма ряда этих солей в растворе ( рис. 140) можно предположить, что анионы образуют только ионные связи и компенсируют свободные заряды в молекуле аквокобаламина. [36]
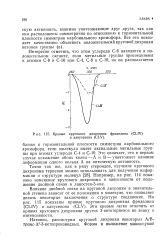 |
Кривые кругового дихроизма фриделина ( CLIV и алнусенона ( CLV. [37] |
Влияние двойной связи на круговой дихроизм в значительной степени зависит от ее положения в молекуле, что позволяет делать некоторые заключения о структуре соединения. Эти кривые легко отличить от кривых кругового дихроизма других 3-кетотерпенов по знаку и интенсивности. [38]
Эффект Коттона часто лучше оценивать из кривых кругового дихроизма. [39]
Особый случай представляет 3-бензоат 5 ( 3, 6 3-эпокси - 7-кето-холестана ( CXI), который имеет кривую кругового дихроизма с двумя максимумами. Предположение о существовании двух равновесных конформаций не вполне обоснованно, так как кривые кругового дихроизма, снятые при различных температурах, в принципе аналогичны кривым для обычных кетонов стероидного ряда. В частности, остается постоянным отношение амплитуд двух компонентов кривой кругового дихроизма. Влияние полярности растворителя также выражено не в большей степени, чем для кетостероидов, имеющих только один оптически активный переход. [40]
Влияние фонового вращения характерно не только для кривых ДОВ кето-соедннений, оно заметно также и для других молекул, содержащих хромофор. Из рисунка непосредственно следует, что, в то время как на кривых ДОВ ( полученных для раствора в метаноле) эффект Коттона заметно не проявляется, на кривых кругового дихроизма для обоих веществ ясно виден положительный эффект Коттона. Клайн и др. [11] предложили правило секторов для п - л - нерехода в лакто-нах. Кроме того, в этом случае достоинство кривых ДОВ состоит в том, что они убедительно показывают, что сильная отрицательная оптическая активность связана с 6-связыо. [41]
Правильная формула не может быть приписана сразу соответствующему изомеру просто путем сравнения с кривыми кругового дихроизма стероидов, так как соединения XXV и XXVI относятся ктрициклическо-му ряду. Однако определение конфигурации этих соединений все-таки возможно, поскольку, как мы видели, знак кругового дихроизма обычно зависит только от ориентации атомов на участке молекулы вблизи сочленения двух колец, что позволяет нам ограничиться рассмотрением сочленения первых двух колец. Кроме того, зеркальные изображения различных ориентации атомов молекулы характеризуются кривыми кругового дихроизма, которые практически являются антиподами по отношению к кривым отображаемых соединений. Формулы XXVe и XXVIfi соответствуют 3-кетостероидам, в которых конфигурации атомов в положениях 5 и 10 являются антиподами по отношению к конфигурациям тех же атомов в природных 3-кетостероидах. Следовательно, знак кругового дихроизма в этом случае должен быть противоположен знаку кругового дихроизма соответствующих природных кетонов. Поскольку соединение XXVB имеет А / В-грамс-сочленение ( 5 3 - Юсе), его круговой дихроизм должен быть отрицательным, в то время как соединение типа XXVIB ( А / В-цмс-сочленение) должно иметь положительный эффект. [42]
При изучении природных соединений часто возникает проблема локализации карбонильной группы в полициклическом скелете молекулы. В ряде случаев метод кругового дихроизма дает простое решение, поскольку в зависимости от положения в стероидном скелете карбонильная группа имеет кривую кругового дихроизма, характеристическую по знаку и форме. [43]
Авторы установили, что природа заместителя X мало влияет на УФ-спектры указанных соединений. Гораздо больше влияние этих групп проявляется в данных кругового дихроизма и дисперсии оптического вращения. Так, для соединений () R3SiH экстремум эффекта Коттона кривой дисперсии оптического вращения лежит при 223 нм, а максимум на кривых кругового дихроизма - при 225 нм; эти значения хорошо совпадают с основным максимумом в УФ-спектре при 225 нм. [44]
Водородная связь сдвигает п - л - переход карбонильной группы в сторону более коротких длин волн, и, следовательно, аналогичным образом изменяется круговой дихроизм рассматриваемых молекул. В целом кривая кругового дихроизма должна иметь форму суммарной кривой. Однако в действительности это не совсем так; если мы примем во внимание различие в амплитуде и величине батохромного сдвига, то увидим, что кривые кругового дихроизма 20-кетопрегнана совмещаются с кривыми кругового дихроизма соответствующих 17а - оксипроиз-водных. [45]
Страницы: 1 2 3 4