Ароматический атом
Cтраница 2
Полоса поглощения 1450 ом 1 может быть вызвана как ароматическими атомами углерода, так и алифатическими. Поглощение при 1380 см-1 вызвано асимметричными деформационными колебаниями СНз-групп. Расщепление данной полосы поглощения в дублет позволяет предполагать наличие в составе молекул пековых материалов гем-диме-тильных лрупп. [16]
Замещение диазогруппы на гидроксигруппу представляет собой реакцию нуклеофильного замещения у ароматического атома углерода и формально может рассматриваться как гидролиз соли диазония. [17]
Фенольное кольцо расположено примерно параллельно основанию пирамиды, а несколько ароматических атомов углерода осуществляют связи с атомом Си, которые значительно короче ( 3 2 - 3 3 А), чем рассчитанные по сумме вандерваальсовых радиусов. Вторая структурная особенность этого комплекса представляет особый интерес в связи с реакцией депротонирования пептидных групп ( разд. Это комплекс такого же типа, как ( CuH iL) 2, но депротонированная пептидная группа лиганда находится по соседству с концом, содержащим карбоксильную группу, а не аминогруппу. Трипептиды образуют пятичленные хелатные кольца с двумя атомами Си, в которых каждый атом Си связан с двумя молекулами лиганда; этим объясняется их димерный состав. [18]
Здесь ао и а - кулоновские интегралы для кислорода и ароматического атома углерода, а Рсо и р - резонансные интегралы карбонильной С-О - связи и ароматической С-С - связи соответственно. Ригер и Френкель [50] показали, что наилучшие значения параметров h и k составляют 1 6 и 1 5 соответственно. [19]
Как известно, в общем случае механизмы реакций замещения у насыщенного, олефинового и ароматического атома углерода существенно отличаются друг от друга. [20]
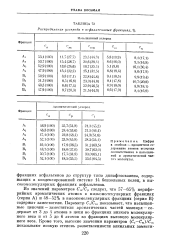 |
Распределение углерода в асфальтеновых фракциях, %. [21] |
Из значений параметров CSJCP следует, что 57 - 65 % периферийных ароматических атомов в низкомолекулярных фракциях ( серия А) и 48 - 52 % в высокомолекулярных фракциях ( серия В) содержат заместители. Параметр Са / С а показывает, что насыщенные цепочки - заместители ароматических частей молекул - содержат от 3 до 4 атомов в цепи во фракциях низкого молекулярного веса и от 5 до 6 атомов во фракциях высокого молекулярного веса. [22]
Параметр общей ароматичности ( степень ароматичности / а, представляющая долю ароматических атомов углерода от общего их количества в смеси) играет существенную роль в структурно-групповом анализе нефтяных фракций. Используемые в практике исследования неспектральные методы ( прямое аналитическое гидрирование и метод п - d - М [13]) обладают рядом существенных недостатков, прежде всего длительностью анализа. Все они основаны на поглощении в области 1600 см-1, отвечающем колебаниям СС связи бензольного кольца, но различаются менаду собой подходом к оценке интенсивности этого поглощения и обработке спектрофо-тометрических данных. [23]
Такой механизм предполагает, что очень скоро после соединения нитроний-иона с ароматическим атомом углерода протон, соединенный с этим атомом, отщепляется. Таким образом этим механизмом исключается тримолекулярнай реакция ] Подтверждение этому авторы видят в том, что, исходя из всей предлоясенгнои ими схемы нитрования, удается вывести кинетические аффекты, которые были экспериментально аайдены при изменении растворителей. Вывод этот сводится к следующему. [24]
Такой механизм предполагает, что очень скоро после соединения нитроний-иона с ароматическим атомом углерода протон, соединенный с этим атомом, отщепляется. Таким образом этим механизмом исключается тримолекулярнай реакция. Подтверждение этому авторй видят в том, что, исходя из веей предложеншои жми схемы нитрования, удается вывести кинетические аффекты, которые быяв экспериментально найдены при изменении растворителей. Вывод этот сводится к следующему. [25]
Трудно предположить, что электроположительная метильная группа, если она связана с ароматическим атомом углерода, станет электроотрицательной, если она связана с азотом или кислородом. В тех случаях, когда отсутствует сопряжение между заместителем и удаленным от него реакционным центром, метилированный заместитель - более сильный донор электронов, чем неметилированный. Так, л-метоксибензойная кислота - более слабая, чем м-оксибензойная. Метильная группа в СН3 - N и СН3 - О обладает положительным индукционным эффектом. [26]
Реакция замещения у ацетиленового атома углерода во многом напоминает кислотное расщепление связи С - Э у ароматического атома углерода. [27]
Для незамещенных кольцевых систем получена серия параллельных линий для зависимости L-Ve, и чем больше число ароматических атомов углерода NQ в молекуле, тем выше расположена линия. При постоянном числе атомов ароматического углерода удерживаемый объем уменьшается с увеличением размера молекулы, но если увеличивается число ароматических атомов углерода, то возрастает и удерживаемый объем. [28]
Дня незамещенных кольцевых систем получена серия параллельных линий для зависимости L-Ve, и чем больше число ароматических атомов углерода NQ ъ молекуле, тем выше расположена линия. При постоянном числе атомов ароматического углерода удерживаемый объем уменьшается с увеличением размера молекулы, но если увеличивается число ароматических атомов углерода, то возрастает и удерживаемый объем. [29]
Поведение нитрогруппы следовало бы рассматривать с учетом того, связана ли она с насыщенным, ненасыщенным или ароматическим атомом углерода. Однако изложение может быть сокращено, если с самого начала выделить ряд общих свойств нитросоединений. Так, во-первых, нитрогруппа в насыщенных соединениях, подобно карбонильной группе, активирует а-во-дородные атомы, которые легко могут отрываться в виде протонов под действием подходящих оснований, причем образующиеся карбанионы будут затем взаимодействовать с простыми карбонильными соединениями или с а р-ненасыщенными системами по реакциям типа альдольной конденсации или конденсации Михаэля. Под действием оснований также легко осуществляется а-галогенирование и другие реакции а-замещения. Во-вторых, в а [ - ненасы - щенных соединениях нитрогруппа направляет реакцию нуклеофильного-присоединения по связи С С таким же образом, как карбонильная или нитрильная группы. В-третьих, в ароматических соединениях нитрогруппа оказывает настолько сильное дезактивирующее и деета-ориентирующее действие, что полностью подавляет такие - реакции, как реакция Фриделя - Крафтса и меркурирование. Все эти - свойства будут кратко проиллюстрированы ниже на примерах, а основное внимание будет уделено наиболее специфичным реакциям для нитросоединений. Изложение разбито на три раздела - нитроалканы, а р-ненасыщенные нитросоединения и ароматические нитросоединения, поскольку реакции нитрогруппы, даже самые простейшие, например восстановление, в очень сильной степени зависят от природы углеводородного остатка, с которым она связана; кроме того, реакции, свойственные собственно нитрогруппе, весьма немногочисленны. [30]
Страницы: 1 2 3 4