Кинетическая кривая
Cтраница 4
Кинетические кривые Д - Р - t окисления таких непредельных углеводородов, как этилен и ацетилен, имеют совсем иной вид, чем в случае окисления предельных углеводородов. Так, Хиншельвуд и Томпсон [45], изучавшие кинетику окисления этилена в статических условиях ( Т 450 С; С2Н4 202) нашли, что прирост давления по ходу реакции не имеет / 5-образного характера. В начале наблюдается небольшой период индукции без видимого изменения начального-давления, затем происходит линейный прирост давления. Скорость реакции, следовательно, после незначительного промежутка времени достигает максимального значения, которое затем только медленно и плавно уменьшается в результате израсходования исходных веществ. [46]
 |
Типы кинетических кривых сорбции. [47] |
Кинетическая кривая 4 характерна для двухстадийного процесса сорбции: быстрое протекание начальной стадии до установления квазиравновесного состояния с формальным подчинением закономерностям нормальной диффузии и последующее замедление сорбции на второй стадии. [48]
 |
Изменение концентрации с одного из исходных веществ в процессе реакции. а-некаталитические и каталитические реакции. б-автокаталитическая реакция. в-взрывная. [49] |
Кинетические кривые изображают найденные из опытов зависимости концентрации выбранного реагента [ см. уравнение ( XVII. [50]
 |
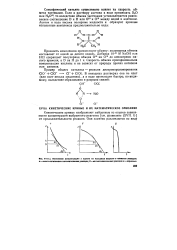
Зависимость степени превращения углеводорода от условного времени контакта при 460 С. [51] |
Кинетические кривые на рис. 5.4 выражают зависимость степени превращения циклогексана, метилциклопентана, пятичленных нафте-нов С7 ( этилциклопентана и диметилциклопентанов), а также суммы гептанов, от условного времени контакта ( обратной величины объемной скорости подачи сырья) при 460 С. [52]
 |
Кажущаяся энергия активации. наж реакций каталитического риформинга. [53] |
Кинетические кривые на рис. 5.5 позволяют приближенно оценить влияние температуры в-янтервале 460 - 500fC на скорости превращения метилциклопентана и суммы гептанов. Аналогичные зависимости для реакций образования бензола и толуола, а также реакций изомеризации н-гексана могут быть получены по данным табл. 5.4. Относительные скорости реакций при разных температурах определяли исходя из того, что они равны относительным скоростям пропускания сырья, при которых достигается заданная степень превращения или равный выход ароматичесфго углеводорода. [54]
Кинетические кривые скорость - время ( и-т) трибореакций обычно характеризуются четырьмя участками: малая постоянная во времени скорость при отсутствии обработки тела; кривая подъема v в начале механического воздействия, высокая v в течение продолжительного периода и спад ее во времени после конца обработки. [55]
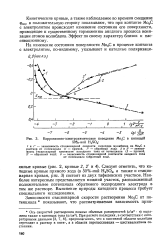 |
Коррозионно-электрохимическое поведение Мо2С в кипящей. [56] |
Кинетические кривые, а также наблюдаемое во времени смещение в положительную сторону показывают, что при контакте Мо2С с электролитом происходит изменение состояния его поверхности, приводящее к существенному торможению анодного процесса ионизации атомов молибдена. Эффект по своему характеру близок к пас-сивационному. [57]
 |
Кинетические кривые реакции первого порядка. Изменение концентрации реагентов ( 7 и продуктов реакций ( 2 в зависимости от времени. [58] |
Кинетическая кривая, отвечающая уравнению (34.4), приведена на рис. НО. [59]
Кинетические кривые как для гомогенных четвертичных фосфониевых и аммониевых солей платины, так и для закрепленных на силикагеле [10] имеют вид, аналогичный полученным для платинированных анионитов. [60]
Страницы: 1 2 3 4 5