Кристалл - щавелевая кислота
Cтраница 2
После уточнения с помощью поиска минимума функционала (3.226) ( где Но тсо определено из уравнений (3.232), (3.233) оценки параметров ( для кристаллов щавелевой кислоты методом случайного поиска) для первой гипотезы приобрели вид / 0 12Лс1 7Л4Кр6, 5 0 657; для второй гипотезы / 0 97Дс 2, 51 872, где S - остаточная сумма квадратов отклонений. [16]
Следует также отметить, что явления соосаждения из растворов с полярными кристаллами изучались значительно чаще, чем с молекулярными, к которым относятся кристаллы щавелевой кислоты. [17]
У обезьян, в течение 3 лет содержавшихся на рационе, включавшем от 0 2 до 0 5 % этиленгликоля, не обнаружилось видимых неблагоприятных последствий; не было выявлено опухолей мочевого пузыря, а только кристаллы щавелевой кислоты и камни. Этиленгликоль, как правило, вызывает умеренное раздражение глаз и кожи, но может абсорбироваться через кожные покровы в количествах, достаточных для отравления. [18]
Поскольку вклад энтальпийной движущей силы весьма существен, то в случае некорректности полученных соотношений (1.243) - (1.247) можно было бы ожидать различных значений е, Ua для роста кристаллов алюмоаммонийных квасцов различных масс и более сильной зависимости коэффициента рм от температуры при растворении кристаллов щавелевой кислоты, чем зависимости коэффициента диффузии от температуры. [19]
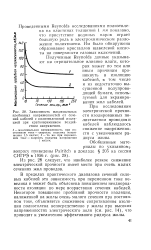 |
Зависимость максимальных пробивных напряженностей от сечений кабелей с полиэтиленовой изоляцией при кратковременном воздействии напряжения. [20] |
Проведенными Reynolds исследованиями полиэтилена на пластинах толщиной 1 мм показано, что присутствие водяных паров играет большую роль в электрохимическом разложении полиэтилена. Им было обнаружено образование кристаллов щавелевой кислоты на поверхности газовых включений. [21]
Затем обратный холодильник заменяют прямым и отгоняют воду и HNO3 до тех пор, пока объем жидкости не станет равным примерно 45 - 50 мл. При охлаждении оставшегося раствора выделяются кристаллы щавелевой кислоты. [22]
Затем обратный холодильник заменяют прямым и отгоняют воду и HNO3 до тех пор, пока объем жидкости не станет равным примерно 45 - 50 мл. При охлаждении оставшегося раствора выделяются кристаллы щавелевой кислоты. [23]
В СССР разработан промышленный способ получения щавелевой кислоты из этиленгдиколя [18], заключающийся в том, что этиленгликоль окисляют смесью азотной ( 23 %) и серной ( 34) кислот в присутствии катализатора - пятиокиси ванадия ( 0 003) Процесс ведут при 70 в течение 7 час. После завершения реакции продукты окисления охлаждают и кристаллы щавелевой кислоты отделяют на центрифуге. Расход этиленгликоля составляет около 600 кг на I т щавелевой кислоты. [24]
Раствор нитрата, хлорида или перхлората тория, свободный от сульфатов и фосфатов, готовят таким образом, чтобы он содержал 100 мг тория или менее на 100 мл раствора и чтобы его нормальность по кислоте составляла 1 - 2 N. Раствор нагревают до кипения и медленно прибавляют либо кристаллы щавелевой кислоты, либо ее насыщенный раствор, так чтобы, по крайней мере, присутствовал 100 % - ный избыток для IN кислого раствора и 400 % - ный - для 2N кислого раствора. Суспензию кипятят несколько минут, снимают с плитки и оставляют на ночь. После фильтрования осадок промывают раствором, содержащим 25 г Н2С204 2Н2О и 20 мл 2N HC1 в 1 л воды. [25]
После прекращения подачи этилена реакция продолжается с выделением окислов азота и завершается тем быстрей, чем выше температура. При 60 - 62 С реакция полностью завершается через 1 - 1 5 ч, а кристаллы щавелевой кислоты выделяются из раствора при его охлаждении до 12 С. [26]
Остаток сплавляют с 0 5 г K2S207 при 600 - 700 С в течение 30 - 40 мин. По охлаждении плав растворяют в 2 5 мл 4 % - ного раствора щавелевой кислоты при слабом нагревании; чтобы избежать выпадения кристаллов щавелевой кислоты, испаряющуюся воду восполняют. [27]
Были проведены эксперименты в пределах температур 303 - 323 К, концентраций 13 - 21 %, при различных массах кристаллов ( 0 2 - - 7 мг) по растворению кристаллов щавелевой кислоты в трубе ячейки. Система уравнений, описывающая движение, растворение кристалла совместно с явлениями тепло - и массообмена, аналогична предыдущей. В [72] исследовалась данная система, в качестве движущей силы было принято пересыщение cih - с, ( растворение идет в диффузионной области), была найдена зависимость Shv4 Re0 5 для определения рм. [28]
В японском патенте [39] описан способ получения щавелевой кислоты из ацетилена, согласно которому ацетилен пропускают через раствор азотной кислоты ( cL 1 3) в смеси с кислородом или воздухом. Реакция ведется в присутствии азотнокислой ртути. Маточник после отделения кристаллов щавелевой кислоты укрепляется и повторно используется для окисления. [29]
После окончания реакции, как уже было сказано, можно было легко выделить тонко размельченную окись осмия нагреванием с небольшим количеством аммиака и профильтровать жидкость. После выпаривания жидкости была получена соль в виде иглообразных призм, группировавшихся в форме звезды вокруг одной общей точки. Более подробным исследованием было легко установлено, что эта соль представляет собою кислый щавелевокислый аммиак, а именно: раствор этой соли при осаждении свинцовым сахаром давал щавелевокислый свинец, при разложении которого сероводородом получались кристаллы чистой щавелевой кислоты, вызывавшей сильное помутнение раствора гипса. [30]
Страницы: 1 2 3