Валентный кристалл
Cтраница 1
Валентные кристаллы, прототипом которых является алмаз характеризуются сильно выраженной направленностью валентностей. Атомы в валентном кристалле стремятся занять строго определенные взаимные положения; энергия решетки сильно зависит от угловой ориентации атомов. Силы связи в этих веществах весьма сходны с силами связи между атомами идеальной органической молекулы. Валентные кристаллы обычно образуют элементы, расположенные в малых периодах периодической системы элементов. Поверхностный слой атомов в валентном кристалле является весьма ненасыщенным, поскольку отсутствует прилегающий слой атомов, с которым могли бы быть связаны атомы поверхности. Поверхностный слой такого типа должен быть чрезвычайно реакционноспособным. Этот слой должен образовывать прочные связи с молекулой, приближающейся к поверхности, в частности в случае, когда прочность связей в молекуле меньше, чем в кристалле. [1]
Валентные кристаллы ( алмаз, карборунд, германий и др.) имеют такое строение кристаллической решетки, при котором число атомов, окружающих данный атом решетки, равно его валентности. Эти кристаллы образуются из легких элементов периодической системы. [2]
Рассмотрим валентный кристалл простого вещества А, содержащий наряду с электронами проводимости и дырками вакансии. [3]
 |
Примесь р-типа ( тетраэдричеокие связи. [4] |
Рассматривая валентные кристаллы IV группы таблицы Менделеева ( алмаз, кремний, германий, серое олово) мы опять сталкиваемся со случаем, рассмотренным в первом разделе: мы имеем решетку идентичных атомов. [5]
В валентных кристаллах вакансии могут быть как донорами, так и акцепторами. В ионных кристаллах анионные вакансии являются, как правило, донорами, а катионные - акцепторами. Сущность происходящих при этом электронных переходов удобно проследить на простейшем примере образования центров окраски в кристаллах галогенидов щелочных металлов. [6]
Инфракрасное поглощение валентных кристаллов, обусловленное примесями. [7]
К числу валентных кристаллов относятся решетки углерода ( алмаза), кремния и германия. Все эти элементы имеют по четыре валентных электрона. [8]
В узлах кристаллической решетки валентных кристаллов расположены нейтральные атомы. [9]
Рассмотрим вопрос применительно к валентным кристаллам. Можно считать, что потенциальная энергия атома в таких кристаллах в основном обусловлена кулоновским отталкиванием остовов и обменным взаимодействием валентных электронов. [10]
Большая часть электронов в валентном кристалле участвует в валентных связях и самостоятельно покидать их не может. [11]
Любая из этих плоскостей представляет собой своеобразный двухмерный валентный кристалл, со ставленный из колец, подобных бензольному. [12]
Также замечено, что образование валентных кристаллов встречает иное препятствие, поскольку оно повлекло бы. [13]
Алмаз является типичным представителем класса валентных кристаллов, у которых координационное число ( в данном слу чае 4) обусловлено числом гомеополярных связей отдельного атома. [14]
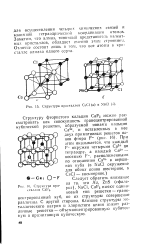 |
Структура кристаллов CsCl ( а и ХаС. ( о.| Структура кристаллов Саг2. [15] |
Страницы: 1 2 3