Более легкий атом
Cтраница 2
В ядрах атомов между протонами как одноименно заряженными частицами, кроме ядерных сил притяжения, должны действовать и электрические силы отталкивания. В более легких атомах эти кулоновские силы отталкивания сравнительно небольшие и подавляются значительно превосходящими их ядерными силами притяжения. Поэтому эти ядра обладают высокой степенью прочности. В тяжелых ядрах, имеющих большое количество протонов, электрические силы отталкивания значительно возрастают и энергия связи на 1 нуклон уменьшается. Если число протонов в ядре превышает 100, ядро теряет свою устойчивость. Это и подтверждают опыты искусственного получения ядер тяжелых элементов, имеющих ничтожно малый период жизни - минуты, секунды. [16]
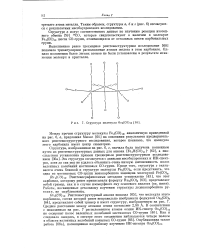 |
Структура молекулы Osa ( COi2. [17] |
Выполненное ранее трехмерное рентгеноструктурное исследование [60] показало триангулярное расположение атомов железа в этом карбониле. Однако положения более легких атомов не были установлены в результате искажения молекул в кристалле. [18]
Так, Na и К, Li и Rb относили к группе щелочных металлов, куда причисляли часто и Т1, а между тем даже у На и К, несмотря на незначительное различие в величине атомного веса, гораздо более различия в свойствах, чем у К, Rb и Cs. Так, хотя натрий имеет более легкие атомы, но он и все его соединения тяжелее калия и соответственных его соединений. [19]
Так, Na и К, Li и Rb относили к группе щелочных металлов, куда причисляли часто и Т1, а между тем даже у Na и К, несмотря на незначительное различие в величине атомного веса, гораздо более различия в свойствах, чем у К, Rb и Cs. Так, хотя натрий имеет более легкие атомы, по он и все его соединения тяжелее калия и соответственных его соединений. Таково же положение Mg по отношению к Са; положение РЬ в отношении к Са, Sr, Ba таково же, то-есть очень сомнительно, как и положение Т1 в отношении К, Rb, Cs. [20]
Так, хотя натрий имеет более легкие атомы, но он и все его соединения тяжелее калия и соответственных его соединений. Так, NaCl и КС1 кристалли зуются в кубах ( КС1 часто в комбинации куба с октаэдром); однако изомерных смесей ни в природе не встречается пи искусственно не получено. В страссфурских залежах встречаются часто кристаллы NaCl и К. Таково же положение Mg по отношению к Са; положение РЬ в отношении к Са, Sr, Ва таково же, тоесть очень сомнительно, как и положение Т1 в отношении К, lib, Cs. [21]
Соединения IC1 и 1С13 играют определенную роль в количественном анализе. Эти полярные молекулярные вещества построены таким образом, что более тяжелый атом координирует вокруг себя более легкие атомы. Всегда нечетное число атомов в молекуле увеличивается при увеличении соотношения радиусов бол / Ямал - Так, атом иода может соединяться с семью атомами фтора, но лишь с одним атомом брома. Бром может координировать самое большое пять атомов другого галогена. Данные по устойчивости межгалогенных соединений, представленные на рис. В. [22]
Группы, в состав которых входит легкий атом водорода: - NH, - ОН, - SH. Валентные и деформационные колебания в такой группе сводятся фактически к перемещению атома водорода, как более легкого атома, и лишь незначительно затрагивают остальную часть молекулы. Кроме этого, названные группы имеют маленькую приведенную массу, благодаря чему их характеристические полосы лежат в высокочастотной области ( выше 3000 см -), где другие группы полос не дают. [23]
 |
Принципиальная схема метода сопла. [24] |
Так как скорость эта при прочих равных условиях тем значительнее, чем меньше масса частицы, более легкие атомы того или иного газообразного элемента проходят сквозь различные мелкопористые перегородки несколько быстрее, чем более тяжелые. В результате пространство перед такой перегородкой временно обогащается тяжелым изотопом, пространство за перегородкой - легким. Многократно повторяя процесс диффузии, удается в конце концов достигнуть весьма полного разделения входящих в состав исходного газа изотопов. [25]
Так как скорость эта при прочих равных условиях тем значительнее, чем меньше масса частицы, более легкие атомы того или иного газообразного элемента проходят сквозь различные мелкопористые перегородки несколько быстрее, чем более тяжелые. В результате пространство перед такой перегородкой временно обогащается тяжелым изотопом, пространство за перегородкой - легким. Многократно повторяя процесс диффузии, удается в конце концов достигнуть весьма полного разделения входящих в состав исходного газа изотопов. [26]
Заметим, что в структуре HgCl2, также с линейными молекулами Cl-Hg-CI, упаковка молекул имеет менее плотный характер н кратчайшее межмолекулярное расстояние Hg... Углы Cl-Hg-CI в структуре HgCL в ряде случаев заметно отклоняются от 90, что вполне согласуется с уже неоднократно отмеченным уменьшением склонности более легких атомов к образованию выравненной системы рст-связен. [27]
Заметим, что в структуре HgCI2, также с линейными молекулами Cl-Hg-Cl, упаковка молекул имеет менее плотный характер и кратчайшее межмолекулярное расстояние Hg... Углы Cl-Hg-Cl в структуре HgCU в ряде случаев заметно отклоняются от 90, что вполне согласуется с уже неоднократно отмеченным уменьшением склонности более легких атомов к образованию выравненной системы ра-связей. [28]
Константа скорости kz имеет различные значения для симметричных и несимметричных молекул. В возбужденных несимметричных молекулах, атомы которых имеют заметно различающиеся массы, например в НС1 или SO, большая часть колебательной энергии приходится на колебание более легкого атома. Следовательно, эффективная дезактивация будет происходить только в тех столкновениях, в которых М подлетает к молекуле со стороны легкого атома. В случае НС1 и HF это равносильно утверждению, что лишь менее половины столкновений оказывается эффективными. [29]
Этот эффект был назван сначала разрушением атома. Однако наблюдения с камерой Вильсона показали, что ct - частица, как правило, застревает в ядре азота, так что в действительности происходит превращение более легкого атома в более тяжелый. Такой же эффект удалось наблюдать примерно на десятке других элементов. [30]
Страницы: 1 2 3 4