Ковалентный кристалл
Cтраница 2
Многие ковалентные кристаллы ( например, германий) плавятся с разрушением направленных связей и переходом в металлическое состояние, соответствующее ОЦК структуре. Наконец, элементы группы кислорода и галогены плавятся без разрушения направленных связей, сохраняя молекулярную структуру в жидком и даже в газообразном состоянии. [16]
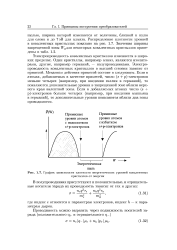 |
График зависимости плотности энергетических уровней ковалентных. [17] |
Электропроводность ковалентных кристаллов изменяется в широких пределах. Одни кристаллы, например алмаз, являются изоляторами, другие, например германий, - полупроводниками. Электропроводность ковалентных кристаллов в высшей степени зависит от примесей. Механизм действия примесей состоит в следующем. Если в атомах, добавляемых в качестве примесей, число ( s р) - электронов меньше четырех ( например, при введении галлия в германий), то появляются дополнительные уровни в запрещенной зоне вблизи верхнего края валентной зоны. Если в добавляемых атомах число ( s р) - электронов больше четырех ( например, при введении мышьяка в германий), то дополнительные уровни появляются вблизи дна зоны проводимости. [18]
Для ковалентных кристаллов с заметной долей ионноста 5р3 - гибридизованные орбитали, описываемые выражениями (3.1), ориентированы в направлениях ближайших соседей и могут быть сконструированы для каждого сорта атомов, образующих кристалл. [19]
 |
Ионные потенциалы некоторых катионов. [20] |
Свойства ковалентных кристаллов существенно отличаются от описанных выше свойств молекулярных веществ. Ковалентные связи в этих веществах образуют непрерывную сетку, связывая все атомы кристалла в протяженный каркас. [21]
 |
Строение кристалла алмаза.| Слоистая решетка графита. [22] |
Для ковалентных кристаллов характерны повышенные твердость, механическая прочность и температуры плавления. [23]
 |
Энергия активации ( U ], критическое напряжение crlip ( 0, сдвига и активационный объем ( V для различных веществ. [24] |
Для ковалентных кристаллов характерны высокие значения U и акр, а активационный объем по порядку величины близок к Ь3 ( Ь - вектор Бюргерса); у металлов с типично металлическим; типом связи, напротив, низкие барьеры для сдвига и очень большой активационный объем. [25]
Для ковалентных кристаллов хорошим приближением является представление о направленности химических связей. [26]
Для ковалентных кристаллов W wqj 2, что равно использованному нами ранее значению в кремнии. [27]
Структура ковалентных кристаллов алмаза, кремния и германия определяется тетраэдрической координацией атомов в результате установления химических связей sps. Каждый атом находится в центре тетраэдра, в вершинах которого расположено четыре других атома. Однако структуру алмаза нельзя получить путем набора таких кубов, поскольку в этом случае каждый атом имел бы восемь ближайших соседей и обладал бы объемноцентриро-ванной решеткой. В алмазной решетке каждый куб, содержащий центрированный тетраэдр, отделен от соседнего центрированного куба нецентрированным кубом такого же размера. Обозначим сторону этого большого куба через а и примем ее за постоянную решетки алмаза. [28]
Для ионных и ковалентных кристаллов характерны случаи, когда атомы примеси имеют другую валентность. Если замещающий атом имеет большую валентность ( например, Са2, замещающий Na в NaCl), то это вызывает точечный дефект ( вакансию) в катионной части структуры, так как сумма положительных и отрицательных валентностей в кристаллах обычно соблюдается весьма точно. [29]
К ковалентным кристаллам относятся многие простые и сложные кристаллические вещества, например алмаз, карбид кремния, нитрид алюминия и др. Ковалентные кристаллы имеют высокие температуру плавления и твердость, малую электропроводность, большие показатели преломления. [30]
Страницы: 1 2 3 4 5