Ковалентный кристалл
Cтраница 4
В ковалентных кристаллах слои, цепочки и пары атомов, образующиеся в результате кова лентной связи, притягиваются друг к другу ван-дер-ваальсовыми силами. У многих ковалентных кристаллов ( сурьма, теллур и др.) и у многих металлов ( алюминии, свинец) связь носит одно временно и ковалентный и металлический характер. [46]
В ковалентном кристалле невозможно выделить отдельную структурную единицу. Весь монокристалл по сути дела представляет собой одну гигантскую молекулу. Кристаллическая структура ковалентных твердых тел полностью определяется природой связей. Координационное число многих известных ковалентных кристаллов равно четырем. Это значит, что каждый атом в кристалле образует четыре направленные ковалентные связи. Направленность связи исключает плотнеишую упаковку кристалла. [47]
В частично ковалентных кристаллах со структурой поваренной соли связи уже не являются локализованными, так что такой кристалл должен описываться некоторым набором валентных структур. Одним из наиболее типичных примеров подобных кристаллов являются кристаллы халькогенидов свинца ( PbS, PbSe и РЬТе; см. разд. [48]
В частично ковалентных кристаллах со структурой поваренной соли связи уже не являются локализованными, так что такой кристалл должен описываться некоторым набором валентных структур. Одним из наиболее типичных примеров подобных кристаллов являются кристаллы халькогенидов свинца ( PbS, PbSe и РЬТе; см. разд. [49]
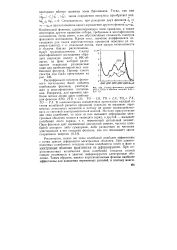 |
Спектр фононного поглощения в QaAs в области энер. ГИЙ 0 04 - 0 07 эВ. [50] |
В гомеополярных ковалентных кристаллах каждый из типов колебаний решетки ( фононов) отдельно не вызывает переменных дипольных моментов и потому не может взаимодействовать со световой электромагнитной волной. [51]
 |
Дефект по Френкелю [ IMAGE ] Образование вакансии.| Примесный атом внедрения.| Примесный атом замещения. [52] |
В ионных и ковалентных кристаллах точечные дефекты электрически активны и могут служить донорами или акцепторами электронов, что создает в кристалле определенный тип проводимости. [53]
 |
Точечные дефекты в кристаллической решетке. [54] |
В ионных и ковалентных кристаллах вакансии и другие точечные дефекты электрически активны и могут быть как донорами, так и акцепторами. Это создает в кристаллах преобладание определенного типа проводимости. В ионных кристаллах электрическая нейтральность кристалла сохраняется благодаря образованию пары точечных дефектов: вакансия-ион, у которых электрические заряды имеют противоположные знаки. [55]
Гомеополярные или ковалентные кристаллы, в которых межатомные связи, в основном ковалентные, относительно немногочисленны. Они обладают изолирующими свойствами как в твердом, так и в расплавленном состоянии ( см., однако, полупроводники, стр. [56]
Почему для ковалентных кристаллов характерны структуры с малым числом ближайших соседей. [57]
Типичным примером ковалентного кристалла является алмаз ( фиг. Все атомы углерода находятся на равных расстояниях друг от друга; каждый из них окружен четырьмя атомами, расположенными в вершинах правильного тетраэдра; вся их совокупность имеет кубическую структуру. Аналогичную структуру имеет цинковая обманка ZnS ( фиг. Так же как и в случае бинарных ионных кристаллов, здесь невозможно различить молекулы углерода или сульфида цинка. [58]
Классическим примером ковалентных кристаллов являются полупроводники Si и Ge, а также С и p - Sn, все это элементы IV группы таблицы Менделеева. У атома углерода С имеются два электрона в s - состоянии и два - в р-состоянии. Однако энергии s - и р-электронов отличаются очень мало, так что при сближении атомов энергетически выгодно перестроиться электронной оболочке атома так, чтобы она соответствовала возбужденному состоянию с 52 ( рис. 4.4, б) с четырьмя электронами с нескомпенсированными спинами. Эти четыре электрона и образуют четыре валентные связи. [59]
 |
Структура алмаза и диоксида кремния. [60] |
Страницы: 1 2 3 4 5